හන්ටිංටන්ගේ රෝගය
| හන්ටිංටන්ගේ රෝගය (HD) | |
|---|---|
| වර්ගීකරණය සහ බාහිර සම්පත් | |
 මධ්ය සකණ්ඨක නියුරෝන (කහ) සහ රෝග ක්රියාවලියේ දී ඇතිවන න්යෂ්ටික අන්තර්ගතයන් (තැඹිලි) දැක්වෙන ආලෝක අන්වීක්ෂීය රූපයක සංස්කරණය කළ සටහනක්; රූපයේ පළල 360 µm | |
| ICD-10 | G10., F02.2 |
| ICD-9 | 333.4, 294.1 |
| OMIM | 143100 |
| DiseasesDB | 6060 |
| MedlinePlus | 000770 |
| eMedicine | article/1150165 article/792600 article/289706 |
| MeSH | D006816 |
| GeneReviews | Huntington Disease |
හන්ටිංටන්ගේ රෝගය (HD) හෙවත් හන්ටිංටන්ගේ කෝරියාව යනුවෙන් හැඳින්වෙන්නේ මොළයේ සෛලවල මරණයට හේතුවන ප්රවේණි ආබාධයකි.[1] මෙහි මුල්කාලීන සංකූලතා ලෙස චිත්තාවේග හෝ මානසික හැකියාවන්ට සියුම් ගැටලු ඇති වේ.[2] ඉන් අනතුරුව සාමාන්යයෙන් සමායෝජනය මඳ වීම සහ නොසන්සුන් ගමන් විලාසය වැනි තත්ත්ව ඇතිවිය හැක.[3] රෝගය වැඩිදියුණු වීමේ දී, සමායෝජනය සිදු නොවී සිරුරේ පාලනය කළ නොහැකි හදිසි චලන ඇතිවනු දැකගත හැක.[2] සමායෝජන චලන අපහසු තත්ත්වයට පත්වන තෙක් කායික හැකියා ක්රමයෙන් අයහපත් අතට හැරේ. එවිට පුද්ගලයාට කථාකළ නොහැකි වේ.[2][3] මානසික හැකියා ක්රමයෙන් පරිහානියට පත්වී චිත්ත වික්ෂේපය හෙවත් ඩිමෙන්ෂියා තත්ත්වයට පත්වේ.[4] පුද්ගලයා අනුව මෙහි විශේෂිත ලක්ෂණ වෙනස් විය හැක.[2] සාමාන්යයෙන් වයස අවුරුදු 30 සහ 50 අතර රෝග ලක්ෂණ ඉස්මතු වන නමුත්, එය ඕනෑම වයසක දී සිදුවිය හැක.[1][4] මෙම රෝගය සෑම අනුප්රාප්තික පරම්පරාවකම දිවියේ මුල් කාලයේ වර්ධනය විය හැක.[2] රෝගීන්ගෙන් 8%ක් පමණ වයස 20ට පෙර සංකූලතා ඉස්මතු වූවන් වන අතර, මෙම රෝග ලක්ෂණ සාමාන්යයෙන් පාකින්සන්ගේ රෝගයට සමානත්වයක් දක්වයි.[4] හන්ටිංටන්ගේ රෝගය සහිත පුද්ගලයින් බොහෝවිට සිය තත්ත්වය අවතක්සේරු කරනු දක්නට ලැබේ.[2]
හන්ටිංටන්ගේ රෝගය දෙමාපියන්ගෙන් දරුවන්ට ආවේණිගත වන රෝගී තත්ත්වයක් වන අතර, රෝගීන්ගෙන් 10%කගේ පමණ මෙය නව විකෘතියක් ලෙස හටගත් තත්ත්වයක් ලෙස හඳුනාගෙන ඇත.[2] මෙම රෝගයට හේතුවන්නේ මිනිසාගේ හන්ටිංටින් නැමැති ජානයේ පිටපත් දෙකෙන් එකක හෝ දෙකෙහිම ඇතිවන අලිංග වර්ණදේහ ප්රමුඛ විකෘතියකි. මින් අදහස් වන්නේ රෝගී පුද්ගලයකුගේ දරුවකුට මෙම රෝගය උරුම වූයේ සම්භාවිතාව 50%ක් බවයි.[1] මෙම හන්ටිංටින් ජානය මගින් "හන්ටිංටින්" යන නාමයම ඇති ප්රෝටීනයකට ප්රවේණික තොරතුර සපයයි.[2] හන්ටිංටින් ප්රෝටීනය සඳහා වන ප්රවේණි කේතයේ CAG (සයිටොසින්-ඇඩිනින්-ගුවැනින්) ත්රික පුනරාවර්තනය වීමෙන් අසාමාන්ය ප්රෝටීනයක් සෑදේ. මෙම අසාමාන්ය ප්රෝටීනය මොළයේ සෛලවලට ක්රමිකව හානි කරයි. මෙය සිදුවන යන්ත්රණය මෙතෙක් සම්පූර්ණයෙන් වටහාගෙන නැත.[1] රෝග ලක්ෂණ දක්නට ලැබුණ ද නොලැබුණ ද, ඕනෑම අවස්ථාවක මෙහි රෝග විනිශ්චය සිදුකරනු ලබන්නේ ප්රවේණි පරීක්ෂාවක් මගිනි.[5] මෙම කරුණ ආචාරධර්මානුකූල විවාදයන්ට හේතු වී ඇත: මෙහි දී පුද්ගලයකු පරීක්ෂාවට තෝරා ගැනීමට තරම් පරිණත යැයි සැලකෙන වයස; සිය දරුවන් පරීක්ෂාවට ලක් කරවීමට දෙමාපියන්ට අයිතිය තිබේ ද යන්න; සහ පරීක්ෂා ප්රතිඵල අනාවරණය සහ රහස්යභාවය ආරක්ෂා කරගැනීම මෙම වාද විෂයයන් වේ.[3]
හන්ටිංටන්ගේ රෝගය සඳහා ප්රතිකාර නොමැත.[1] රෝගයේ පසුකාලීන අවධි සඳහා පූර්ණ-කාලීන සාත්තු කිරීම වැදගත් වේ.[3] ප්රතිකාර මගින් ඇතැම් සංකූලතා මගහැරවිය හැකි අතර, ජීවිතයේ ගුණාත්මය වැඩිදියුණු කළ හැක. චලන ගැටලු සඳහා හොඳම ප්රතිකාරය ලෙස ටෙට්රාබෙනැසින් භාවිතා වේ.[4] සාමාන්යයෙන් යුරෝපීය සම්භවයක් ඇති පුද්ගලයින් 100,000 කට හන්ටිංටන් රෝගීන් 4 සිට 15 දක්වා ප්රමාණයක් හමුවේ.[2][4] මෙම රෝගය ජපනුන් අතර විරළ අතර, අප්රිකාව තුළ නොහඳුනන ශීඝ්රතාවකින් පවතියි. මෙම රෝගය කාන්තාවන් මෙන්ම පිරිමින්ට ද එකසේ බලපායි.[4] නියුමෝනියාව, හෘද රෝග සහ ඇදවැටීමෙන් සිදුවන කායික හානි වැනි සංකූලතාවන් මෙම රෝගීන්ගේ ආයු අපේක්ෂාව අඩු කරයි. මෙම රෝගීන්ගේ මරණවලින් 9%ක් පමණම දිවි නසා ගැනීම් නිසා සිදුවේ.[4] සාමාන්යයෙන් රෝගය පළමුවරට අනාවරණය කරගත් දිනයේ සිට වර්ෂ පහළොවේ සිට විස්ස දක්වා කාලය තුළ රෝගියාගේ මරණය සිදුවිය හැක.[1]
මෙම රෝගය පිළිබඳ යැයි සිතිය හැකි පළමු විස්තරය හමුවන්නේ 1841දී චාල්ස් ඔස්කාර් වෝටර්ස්ගේ වාර්තාවකිනි. මෙම තත්ත්වය පිළිබඳ වැඩිදුර විස්තර කොට ඇත්තේ 1872දී ජෝර්ජ් හන්ටිංටන් විසිනි. ඔහුගේ නාමය අනුව මෙම රෝගය නම්කොට ඇත.[6] 1993දී අන්තර්ජාතික සහයෝගීත්වය ඇතිව ආවේණීය රෝග පදනමේ ප්රධානත්වයෙන් මෙහි ජානමය පදනම හෙළි කරගැනිණි.[7][8] මහජන දැනුවත්භාවය ඇති කිරීමටත්, රෝගීන්ට සහ ඔවුන්ගේ පවුල්වලට සහාය වීම පිණිසත් පර්යේෂණ සහ සහාය සංවිධාන බිහිවන්නට වූයේ 1960 දශකයේ පසුකාලයේ ය.[8][9] වර්තමානය වන විට, රෝගයේ යන්ත්රණය නිශ්චිතව නිර්ණය කිරීම සඳහා සත්ත්ව නිදර්ශන භාවිතයෙන් පර්යේෂණ මෙහෙයවනු ලැබේ. එසේම රෝගය ව්යාප්ත වීම ප්රමාද කිරීමටත්, සංකූලතාවන්ට ප්රතිකාර කිරීමටත් ඖෂධ අත්හදා බැලීම සිදුවේ. රෝගයෙන් ඇතිවූ හානිය පිළිසකර කිරීමේ අරමුණින් යුතුව පියවි සෛල චිකිත්සාව වැනි ක්රමවේද පිළිබඳ නූතන අවධානය යොමුව ඇත.[7]
ලක්ෂණ සහ සංකූලතා
[සංස්කරණය]| උත්කෝප්යතාව | 38–73% |
| උදාසීනභාවය | 34–76% |
| සාංකාව | 34–61% |
| අවපීඩන ගතිය | 33–69% |
| ග්රස්තිය සහ වළක්වාගත නොහැකි ස්වභාවය | 10–52% |
| සයිකෝසියා | 3–11% |
හන්ටිංටන්ගේ රෝගයේ සංකූලතාවන් වඩාත් පැහැදිළිව දර්ශනය වන්නේ වයස අවුරුදු 35 සහ 44 අතර කාලයේ ය. නමුත් එය බිළිඳු වියේ සිට මහලු විය දක්වා ඕනෑම අවධියක ආරම්භ විය හැක.[11][12] මුල් අවධිවල පෞරුෂත්වයේ, ප්රජානනයේ සහ කායික හැකියාවල සියුම් විපර්යාසයන් ඇතිවේ.[11] කායික සංකූලතා මුලින්ම හඳනාගත හැකි අතර, ප්රජානන සහ චර්යාත්මක සංකූලතා[13] සාමාන්යයෙන් මුල් අවධිවල පැහැදිළිව හඳුනාගත නොහැක.[11] හන්ටිංටන් රෝගයෙන් පෙළෙන සියලු දෙනාම ක්රමිකව සමාන කායික සංකූලතා පෙන්වූව ද, ප්රජානන හා චර්යාත්මක සංකූලතා ආරම්භ වීම, ඒවායේ වෘද්ධිය සහ ප්රමාණය පුද්ගලයා අනුව වෙනස් විය හැක.[14][15]
මෙම රෝගී තත්ත්වයේ වඩාත් ලාක්ෂණික මූලික කායික රෝග ලක්ෂණයක් ලෙස කෝරියා යනුවෙන් හඳුන්වන සිරුරේ ඇතිවන සරල, අහඹු, පාලනයෙන් තොර චලන හැඳින්විය හැක.[11] කෝරියාව ඇතැම්විට නොසන්සුන්තාවය, සියුම් අනභිප්රායික චලන, සමායෝජනය මඳවීම හෝ ධ්රැත අක්ෂි චලන ලෙස ආරම්භ විය හැක.[11] මෙවැනි සුළු චාලක අසාමාන්යතාවන් අවම වශයෙන් වසර තුනක් පමණ ඇතුළත විශාල චාලක දුෂ්කෘත්යයන් දක්වා වර්ධනය විය හැක.[14] ආබාධය වර්ධනය වීමේ දී, දැඩි බව, මානසික අසහනය සහ අසාමාන්ය ඉරියව් වැනි ලක්ෂණ පැහැදිළිව දක්නට ලැබේ.[16] ඉහත ලක්ෂණ මොළයේ පිහිටන චලන සඳහා වැදගත් පද්ධතිය වෙත බලපෑමක් සිදුව ඇති බවට සංඥාවකි.[17] මනෝචාලක කෘත්යයන් ශීඝ්රයෙන් පරිහානියට ලක්වන අතර පේශී චලන පාලනයට අවශ්ය ක්රියාවන් කෙරෙහි බලපෑම් ඇතිවේ. සාමාන්යයෙන් මෙහි ප්රතිඵල ලෙස කායික අසමතුලිතතාවය, අසාමාන්ය මුහුණේ ප්රකාශනය, සහ සැපීමේ, ගිලීමේ, හා කථන අපහසුතා ඇතිවේ.[16] ආහාර ගැනීමේ අපහසුතා හේතුවෙන් බොහෝවිට දේහ බර අඩුවන අතර, මන්දපෝෂණයට හේතුවිය හැක.[18][19] නිඳන බාධාවන් ද මෙම රෝග ලක්ෂණ හා සම්බන්ධ ය.[20] බාලක හන්ටිංටන්ගේ රෝගය ඉහත රෝග ලක්ෂණවලින් තරමක් වෙනස් වේ. එය සාමාන්යයෙන් වඩා ශීඝ්රයෙන් ප්රතිචාර දක්වයි. එහි කෝරියාව කෙටිකාලීනව දක්නට ලැබෙන අතර දැඩි භාවය ප්රමුඛ රෝග ලක්ෂණයක් ලෙස පවතියි. අපස්මාර තත්ත්වයන් ද හන්ටිංටන්ගේ රෝගයේ ඉහත ආකාරයේ පොදු ලක්ෂණයකි.[16]
මෙම රෝගී තත්ත්වයේ දී ප්රජානන හැකියා වඩාත් අඩුවීම සිදු වේ.[17] මෙහි දී සැපසුම්කරණය, ප්රජානන නම්යතාව, සාරාංශ චින්තනය, නීති අත්කරගැනීම, සුදුසු ක්රියාමාර්ග ඇරඹීම සහ අයෝග්ය ක්රියාමර්ගවලින් වැළකීම වැනි විධායක ක්රියාවන් කෙරෙහි වැඩි බලපෑමක් සිදුවේ.[17] රෝගය වර්ධනය වන විට, මතකය ක්රමයෙන් ඌන වී යන බැව් පෙනේ. වාර්තාගත හානිය කෙටි කාලීන මතක ඌනතාවේ සිට දිගු කාලීන මතක ඌනතාව දක්වා පරාසයක වූ ආබාධ ඇතිවිය හැක. එසේම ප්රසාංගික (පුද්ගලයකුගේ දිවිය පිළිබඳ මතකය), ක්රියාවලික (යම් කාර්යයක් සිදු කිරීමට සිරුරේ ඇති මතකය) සහ කාරක මතකය ඌන වී යා හැක.[17] ප්රජානන ගැටලු ක්රමයෙන් උග්ර අතට හැරෙන අතර, අවසානයේ ඩිමෙන්ෂියාව ඇතිවිය හැක.[17] ඇල්ෂයිමර්ගේ රෝගය වැනි දර්ශීය බාහික ඩිමෙන්ෂියා තත්ත්වයන්ගෙන් වෙන්කර හඳුනාගැනීමට මෙලෙස සිදුවන පරිහානි තත්ත්වය උපබාහික ඩිමෙන්ෂියා සහලක්ෂණය ලෙස නම්කොට ඇත.[17]
වාර්තාගත ස්නායුකමනෝචිකිත්සීය ලක්ෂණයන් ලෙස සාංකාව, විෂාදය, හැඟීම් ප්රකාශනය මඳ වීම, ආත්මකේන්ද්රීයභාවය, ප්රචණ්ඩභාවය, සහ බලකිරීමේ ස්වභාවය හඳුනාගත හැක. මෙහි අවසානයට සඳහන් ලක්ෂණය නිසා මත්පැනට ඇබ්බැහි වීම, සූදුවෙහි නිරත වීම, සහ අතිලිංගිකතාව වැනි ඇබ්බැහි වීම් උග්ර විය හැක.[10] සෙසු පුද්ගලයින්ගේ ඍණාත්මක ප්රතිචාර හඳුනාගැනීමේ දුර්වලතා ද මොවුන් තුළින් දැකගත හැක.[17] මෙම රෝග ලක්ෂණවල පැවැත්ම අධ්යයනවල අතිශයින් විවිධත්වයක් පෙන්වයි. ජීවිත කාලය තුළ මානසික ආබාධ පැවතීමේ ඇස්තමේන්තුගත ප්රතිශතය 33% සහ 76% අතර වේ.[10] බොහෝ රෝගීන්ට සහ ඔවුන්ගේ පවුල්වලට මෙම රෝග ලක්ෂණ කටුක අත්දැකීමක් වනුයේ, එය බොහෝ දෛනික ක්රියාකාරකම් සහ කායික මානසික තත්ත්වයන් කෙරෙහි බලපාන බැවිනි.[10] සාමාන්ය ජනගහනයට සාපේක්ෂව මොවුන් අතර සියදිවි නසා ගැනීමේ සිතිවිලි සහ උත්සාහයන් වඩාත් බහුල ය.[11] කෝරියාව පිළිබඳ බොහෝ පුද්ගලයින්ගේ දැනුම මඳ වී තිබේ.[21]
විකෘති වූ හන්ටිංටින් ජානයේ ප්රකාශනය සිරුර පුරාම දක්නට ලැබෙන අතර, එය එය ඍජුවම මොළයෙන් පිටත පිහිටි පර්යන්ත පටකවල අසාමාන්යතාවන්ට හේතුවේ. මෙම අසාමාන්යතාවන් අතර පේශි ක්ෂය වීම, හෘත් අකරණිය, ග්ලූකෝස්වලට සංවේදීභාවය මඳ වීම, බර අඩුවීම, අස්ථිවෛවර්වය, සහ වෘෂණ ක්ෂීණ වීම නැකි තත්ත්වයන් වේ.[22]
ප්රවේණි විද්යාව
[සංස්කරණය]සෑම මිනිසකු සතුවම හන්ටිංටින් ජානයේ (HTT) ජානයේ පිටපත් දෙකක් දක්නට ලැබේ. මේවා හන්ටිංටින් ප්රෝටීනයට (HTT) ප්රවේණි කේතය සපයයි. මෙම ජානය HD සහ IT15 ලෙස ද හඳුන්වනු ලැබේ. IT15 යන්නෙන් අදහස් වන්නේ 'ප්රයෝජනවත් පිටපත 15' (interesting transcript 15) යන්නයි. මෙම ජානයේ කොටසක් ට්රයිනියුක්ලියෝටයිඩ පුනරාවර්තී කොටසකින් සමන්විත ය. මෙහි දිග එක් එක් පුද්ගලයා අනුව වෙනස් වන අතර, පරම්පරා අනුව ද දිග වෙනස් විය හැක. නිරෝගී ජානයක මෙම පුනරාවර්තනය දක්නට ලැබේ නම්, ගතික විකෘතියක් හේතුවෙන් පුනරාවර්තී ප්රමාණය වැඩි කර, දෝෂ සහගත ජානයක් ඇති කරයි. මෙම පුනරාවර්තී කොටසේ දිග නියමිත දේහලිය අගයයක් කරා ළඟාවන විට, එමගින් විකෘති හන්ටිංටින් ප්රෝටීනය (mHTT) නැමැති විකෘත ප්රෝටීනයක් නිපදවයි. මෙම ප්රෝටීනයේ කෘත්යයන් වෙනස් වීම හේතුවෙන් රෝග ලක්ෂණවලට හේතුවන ව්යාධිවේදීය විපර්යාසයන් දක්නට ලැබේ. හන්ටිංටන්ගේ රෝගයේ විකෘතිය ප්රවේණිකව ප්රමුඛ අතර සම්පූර්ණයෙන්ම වාගේ නිවේධනය වීම (penetrant) සිදුවේ. මේ නිසා පුද්ගලයාගේ HTT තනි ඇලීලයක සිදුවන විකෘතිය පවා රෝගය ඇතිවීමට හේතුවේ. මෙය ලිංගය අනුව ආවේණිගත නොවන්නකි. නමුත් ජානයේ පුනරාවර්තී කොටසේ දිග කෙරෙහි ආසාදිත දෙමාපියාගේ ලිංගය බලපෑ හැක.[23]
ප්රවේණි විකෘතිය
[සංස්කරණය]ට්රයිනියුක්ලියෝටයිඩ පුනරාවර්තී ආබාධ කිහිපය අතුරින් එකක් වන හන්ටිංටන්ගේ රෝගය, ජානයේ පුනරාවර්තී කොටසේ දිග සාමාන්ය පරාසය ඉක්මවා යාම නිසා ඇතිවේ.[24] HTT ජානය පිහිටියේ 4වන වර්ණදේහයේ කෙටි බාහුවේ[24] 4p16.3 පිහිටුමේ ය. HTT ජානය සතුව සයිටොසින්-ඇඩිනින්-ගුවැනින් (CAG) ලෙස පිහිටන DNA භෂ්ම ත්රිත්වයකින් යුත් අනුපිළිවෙලක් ඇත. මෙය බොහෝ වරක් පුනරාවර්තී ලෙස යෙදේ. (උදා ... CAGCAGCAG ...) මෙය ට්රයිනියුක්ලියෝටයිඩ පුනරාවර්තනයකි.[24] CAG යනු ග්ලූටැමීන් නැමැති ඇමයිනෝ අම්ලය සඳහා වන ත්රික ප්රවේණි කේතය (කෝඩෝනය) වේ. මේ නිසා මෙවැනි ත්රික මාලාවක් මගින් පොලිග්ලූටැමීන් පථය (හෙවත් polyQ පථය) නැමැති ග්ලූටැමීන් දාමය සෑදේ. එලෙස ඇතිවන ජානයේ පුනරාවර්තී ප්රදේශය PolyQ කලාපය නම් වේ.[25]
| පුනරාවර්තන සංඛ්යාව | වර්ගීකරණය | රෝගී තත්ත්වය | ප්රජනිතයන්ට ඇති අවදානම |
|---|---|---|---|
| <26 | සාමාන්ය | රෝගී නොවේ | නැත |
| 27–35 | අතරමැදි | රෝගී නොවේ | වැඩියි නමුත් <<50% |
| 36–39 | නිවේධනය වීම අඩු ය | රෝගී විය හෝ නොවිය හැක | 50% |
| 40+ | සම්පූර්ණයෙන් නිවේධනය වේ | රෝගියෙකි | 50% |
සාමාන්යයෙන්, මිනිසා සතුව සෛලප්ලාස්මික හන්ටිංටින් ප්රෝටීනය නිපදවීමට හේතුවන polyQ ප්රදේශයේ ග්ලූටැමින් පුනරාවර්තන 36ට අඩු සංඛ්යාවක් පිහිටයි.[24] කෙසේනමුත්, ග්ලූටැමින් 36 හෝ ඊට වඩා වැඩි ප්රමාණයක් පිහිටීම හේතුවෙන් වෙනස් ලක්ෂණ සහිත ප්රෝටීනයක් සෑදේ.[24] මෙම විපර්යාසයට ලක්වූ ප්රභේදය, විකෘති හන්ටිංටින් (mHTT) නම් වන අතර, එමගින් ඇතැම් නියුරෝන ආකාර ක්ෂය වී යන වේගය වැඩි කරයි. මෙවැනි ආකාරවල නියුරෝන විවිධ ප්රමාණවලින් අන්තර්ගත මොළයේ ප්රදේශ මින් බලපෑමට ලක්වේ.[16] සාමාන්යයෙන්, CAG පුනරාවර්තන සංඛ්යාව මෙමගින් බලපෑම් වන ප්රමාණය කෙරෙහි බලපායි. රෝග ලක්ෂණවල ආරම්භය, 60%ක් පමණම වයසේ විවිධත්වය අනුව විචලනය වන්නේ මේ නිසායි. සෙසු ප්රභේදන පාරිසරික සාධක සහ හන්ටිංටන්ගේ රෝගයේ යන්ත්රණය වැඩිදියුණු කරන ජාන හා සම්බන්ධ ය.[24] පුනරාවර්තන 36–39 අතර සංඛ්යාවක් තිබීම හේතුවෙන් රෝගයේ ඌනිත-නිවේධනයක් පෙන්වයි. මෙවිට රෝග ලක්ෂන ආරම්භ වීම තරමක් ප්රමාද වන අතර, රෝග ලක්ෂණ වර්ධනය වීම ද සෙමෙන් සිදුවේ. ඇතැම් අවස්ථාවල, රෝගය ඇතිවීම බෙහෙවින් ප්රමාද වන අතර, එවිට රෝග ලක්ෂණ කිසිදින හඳනාගත නොහැකි වේ.[26] පුනරාවර්තී ගිණීම් විශාල සංඛ්යාවක් ඇති විට, හන්ටිංටන්ගේ රෝගය පූර්ණ වශයෙන් නිවේධනය වන අතර, වයස අවුරුදු 20දී පමණ එය ආරම්භ විය හැක. මෙවිට මෙම තත්ත්වය බාලක HD, හන්ටිංටන් රෝගයේ අචලක-දෘඪ (akinetic-rigid) හෝ වෙස්ට්ෆැල් ප්රභේදයක් ලෙස හඳුන්වනු ලැබේ. මෙය හන්ටිංටන් රෝගයේ වාහකයන් 7%ක් පමණ සඳහා අදාළ වේ.[27]
ප්රවේණිය
[සංස්කරණය]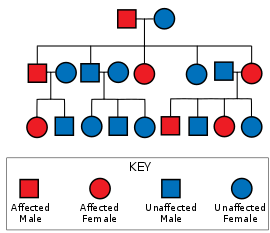
හන්ටිංටන්ගේ රෝගය සතුව අලිංග වර්ණදේහ ප්රමුඛ ආවේණි රටාවක් දක්නට ලැබේ. එනම් රෝගියකුගෙන්, ආසාදිත පුද්ගලයාට සාමාන්යයෙන් ප්රසාරිත ට්රයිනියුක්ලියෝටයිඩ පුනරාවර්තනය සහිත ජානයේ එක් පිටපතක් (විකෘති ඇලීලයක්) උරුම වේ.[11] මෙම විකෘතියේ නිවේධනය වීම අතිශයින් ඉහළ නිසා, විකෘති ජානයේ පිටපතක් සහිත පුද්ගලයින් රෝගී වේ. මෙම ප්රවේණි රටාව තුළ, රෝගියකුගෙන් ඔහුගේ දරුවකුට මෙම විකෘති ඇලීලය උරුම වීමේ 50%ක් අවදානමක් ඇත. එමනිසා එම දරුවන් ද ආබාධය නිසා රෝගී වේ. (රූප සටහන බලන්න) මෙහි සම්භාවිතාව ලිංගය මත රඳා නොපවතී.[28]
ට්රයිනියුක්ලියෝටයිඩ CAG පුනරාවර්තන සංඛ්යාව 28ට වැඩියෙන් පැවතීම ස්වයං ප්රතිවලිතයේ දී අස්ථායී වේ. මෙම අස්ථායී බව නිසා පවතින පුනරාවර්තන ඒකක සංඛ්යාව වැඩි වීම සිදුවේ.[26] ට්රයිනියුක්ලියෝටයිඩ පුනරාවර්තනවල සර්වසම පිටපතක් නිපදවනු වෙනුවට මෙහි දී, පරම්පරාවක් ගතවන විට නව ව්යාප්තියක් (ගතික විකෘති) සෑදීම සිදුවේ.[24] මේ නිසා අනුප්රාප්තික පරම්පරාවල දී පුනරාවර්තන ඒකක සංඛ්යාව වෙනස් වේ. මේ නිසා පුනරාවර්තන ඒකක "අතරමැදි" සංඛ්යාවක් (28–35) හෝ "ඌනිත නිවේධනයක්" (36–40) පෙන්වන රෝගී නොවන දෙමාපියකුගේ ජානයක් සම්ප්රේෂණය වීමේ දී එම ජානයේ පිටපත් සංඛ්යාව වැඩි වීමෙන් පූර්ණ නිවේධන හන්ටිංටන් රෝගියකු බිහි විය හැක.[24] මෙලෙසින් අනුප්රාප්තික පරම්පරාවල පුනරාවර්තන ඒකක සංඛ්යාව (සහ රෝගයේ දරුණුභාවය) ක්රමයෙන් වැඩිවීම ප්රවේණික පූර්වාපේක්ෂණය ලෙස හඳුන්වයි.[24] මෙහි දී අණ්ඩෝද්භවයට සාපේක්ෂව ශුක්රාණුජනනයේ දී ප්රවේණි අස්ථායීභාවය ඉහළ ය.[24] මේ නිසා මාතෘ පාර්ශ්වයෙන් උරුම වන ඇලීල සාමාන්යයෙන් සමාන පුනරාවර්තී දිගකින් සමන්විත වුව ද, පීතෘ පාර්ශ්වයෙන් උරුමවන ඒවායේ දිග වැඩි වීමේ ඉහළ හැකියාවක් පවතී.[24][29] දෙමාපියන්ගෙන් එක් අයකුටවත් CAG පුනරාවර්තන ඒකක 36කට අධික සංඛ්යාවක් නොපිහිටිය ද, හන්ටිංටන් රෝගය නව විකෘතියක් ලෙස ඇති වන අවස්ථා විරළ ය.[30]
ඉතා කලාතුරකින් ප්රසාරිත HD ජානය අන්තර්ගත දෙමාපියන් දෙදෙනකු සිටින අවස්ථාවල, මෙම අවදානම 75% දක්වා ඉහළ යා හැක. දෙමාපියන්ගෙන් එක් අයකුට හෝ මෙම ප්රසාරිත පිටපත් යුගලක් පිහිටයි නම්, මෙම අවදානම 100%කි. (සියලු දරුවන් රෝගී වේ) ජාන යුගළම විකෘති වූ පුද්ගලයින් විරළ ය. එක්තරා කාලයක දී සිතා සිටියේ හන්ටිංටන්ගේ රෝගයේ දෙවන විකෘති ජානය රෝග ලක්ෂණ සහ රෝගය වර්ධනය වීම කෙරෙහි බලනොපාන බවයි.[31] නමුත් එයට රූපානුදර්ශය සහ රෝගය වර්ධනය වීමේ වේගය කෙරෙහි බලපෑ හැකි බව සොයාගෙන තිබේ.[24][32]
යන්ත්රණය
[සංස්කරණය]හන්ටිංටින් ප්රෝටීනය වෙනත් ප්රෝටීන 100කට අධික සංඛ්යාවක් සමග අන්තර්ක්රියා කරයි. එය බහුවිධ ජෛවවිද්යාත්මක කෘත්යයන් කෙරෙහි බලපාන බව පෙනේ.[33] මෙම විකෘති ප්රෝටීනයේ හැසිරීම මෙතෙක් පැහැදිළිව වටහාගෙන නොමැත. නමුත් එය විශේෂයෙන්ම මොළයේ සෛල වැනි සෛල ආකාර කිහිපයකට විෂ සහිත වේ. මුල්කාලීන හානිය striatum ප්රදේශයේ හඳුනාගත හැක. නමුත්, රෝගය වර්ධනය වන විට, මොළයේ සෙසු ප්රදේශ ද පැහැදිළිව බලපෑමට ලක්වේ. මුල්කාලීන රෝග ලක්ෂණ striatum ප්රදේශයේ සහ එහි බාහික සම්බන්ධක පෙදෙස් හා අදාළ වේ. විශේෂයෙන්ම එය චලන පාලනය, චිත්තාවේග සහ උසස් ඥානමය කෘත්යයන් හා සම්බන්ධ ය.[23] හන්ටිංටන් රෝගයේ දී DNA මෙතිල්කරණය ද වෙනස් වී ඇති බව දක්නට ලැබේ.[34]
හන්ටිංටින් කෘත්යය
[සංස්කරණය]සියලු ක්ෂීරපායී සෛලවල HTT ජානය ප්රකාශ වේ. මෙහි ඉහළම සාන්ද්රණයෙන් යුතුව මොළයේ සහ වෘෂණ වලත්, සාමාන්ය ප්රමාණවලින් අක්මාව, හෘදය, සහ පෙනහැලිවලත් හමුවේ.[23] මිනිසුන් තුළ HTTහි කෘත්යය පැහැදිළි නැත. මෙය පිටපත් කිරීම, සෛල සංඥාකරණය, සහ අන්තර්සෛලීය පරිවහනය හා සම්බන්ධ ප්රෝටීන සමග අන්තර්ක්රියා කරයි.[23][35] සතුන් තුළ නම් හන්ටිංටන් රෝගය දැකගැනීමට ඔවුන්ව ප්රවේණිකව විකරණය කළ යුතු ය. ඔවුන්ගේ HTTහි කෘත්යයන් කිහිපයක් හඳුනාගෙන ඇත.[36] මෙම සත්ත්වයින් තුළ, HTT ජානය කලල වර්ධනයට වැදගත් වන අතර, එය නොමැති වීමෙන් කලලයේ මරණය සිදු විය හැක. සෛල විනාශ වීම උත්ප්රේරණය කරන කැස්පේස් එන්සයිමය ක්රියාකාරී වන්නේ මෙම විකෘති ජානය මගින් යුබික්වියින්-ප්රෝටියේස් පද්ධතියට හානි කිරීම නිසා යැයි විශ්වාස කෙරේ. එසේම එම ජානය ක්රමලේඛිත සෛල මරණය වැළැක්වීමේ ප්රති-සෛල විනාශනකාරකයක් ලෙස ක්රියා කරයි. එසේම එමගින් ස්නායු ජනනයේ දී නියුරෝනවල වර්ධනය යාමනය කිරීමට සහ නියුරෝන ආරක්ෂා කිරීමට හේතුවන මොළ-ව්යූත්පන්න නියුරොට්රොෆික සාධකය නැමැති ප්රෝටීනය නිපදවීම පාලනය කරයි. මීට අමතරව HTT ජානය ආශයික පරිවහනය සහ උපාගම සම්ප්රේෂණය සඳහා ආධාර වන අතර, එමගින් ස්නායුක ජාන ප්රතිලේඛනය පාලනය කරයි.[36] HTT ජානයේ ප්රකාශනය ඉහළ ගිය විට සහ වඩවඩාත් HTT නිපදවෙන විට, මොළයේ සෛල පැවැත්ම වැඩිදියුණු වන අතර, mHTTහි බලපෑම් අවම වීම සිදුවේ. එලෙසම HTTහි ප්රකාශනය අඩු වන විට, ප්රතිඵල ලෙස ඇතිවන ලක්ෂණ mHTTහි පැවැත්මෙන් ඇති වන තත්ත්වයනට සමාන වේ.[36] මිනිසුන් තුළ, සාමාන්ය ජානයේ ප්රවිදාරණය රෝගය ඇතිවීමට හේතු නොවේ.[23] සාමාන්යයෙන් විශ්වාස කෙරෙන්නේ HTT ප්රමාණවත් පරිදි සංස්ලේෂණය නොවීම රෝගය ඇතිවීමට හේතු නොවන බවත්, එය mHTTහි ධූලක කෘත්යයක් හේතුවෙන් වර්ධනය වන බවත් ය.[23]
සෛලීය විපර්යාසයන්
[සංස්කරණය]
mHTT හි ධූලක ක්රියාව හේතුවෙන් හන්ටිංටන්ගේ රෝගය සෑදීමේ දී බහුවිධ සෛලීය විපර්යාසයන් සිදු වේ.[37][38] mHTTහි පශ්චාත්ප්රතිලේඛන විකරණ ජෛවීය ක්රියාවලියේ දී, ප්රෝටීන භේදනය නිසා පොලිග්ලූටැමින්වලින් සැදි කෙටි ඛණ්ඩ සෑදිය හැක.[37] ග්ලූටැමීන්හි ධ්රැවීය ස්වභාවය නිසා, විකරණය නොකළ HTT ප්රෝටීන හෝ HTT භේදනයේ දී සෑදෙන HTT ඛණ්ඩ අතර ග්ලූටැමීන් අතිශය සුලබ වන විට, සෙසු ප්රෝටීන සමග අන්තර්ක්රියා සිදුවේ. මේ නිසා, mHTT අණු පට එකිනෙක අතර හයිඩ්රජන් බන්ධන ඇතිවේ. මෙලෙසින් නැවී කෘත්යමය ප්රෝටීන සෑදෙනු වෙනුවට ප්රෝටීන සමාහාරයක් නිර්මාණය වේ.[39] කාලයක් පුරා මෙම සමාහාර එක්රැස් වන විට, මෙම ඛණ්ඩවලට දිගහැරීමට සහ හා වීමට හැකියාව පවතින නිසා අවසානයේ නියුරෝනයේ කෘත්යයට බාධා වේ. මෙම ක්රියාවලිය ප්රෝටීන සමාහරණය නම් වන අතර මෙහි දී, සෛල තුළ අන්තර්ගත දේහ සෑදේ.[37][39] නියුරෝනවල ඇති වන මෙම අන්තර්ගත වක්රාකාරයෙන් බාධා ඇති කරයි. අන්තර්ගත දේහයන් සෛල න්යෂ්ටියේ මෙන්ම සෛල ප්ලාස්මයේ ද දැකගත හැක.[37] මොළයේ සෛල තුළ පිහිටන අන්තර්ගත දේහ මුල්කාලීන ව්යාධිවිද්යාත්මක විපර්යාසයක් ලෙස සැලකේ. ඇතැම් පර්යේෂණවලින් අනාවරණය වී ඇත්තේ ඒවා සෛලයට විෂ විය හැකි බවයි. නමුත් සෙසු පර්යේෂණවලින් පෙනීගොස් ඇත්තේ ඒවා සිරුරේ ආරක්ෂක යන්ත්රණයේ කොටසක් ලෙස ක්රියා කරමින් සෛල ආරක්ෂා කිරීමට උපකාරී වන බවයි.[37]
mHTT නිසා සෛලයේ මරණය සිදුවිය හැකි ආකාර කිහිපයක් හඳුනාගෙන ඇත. මේ අතරට පහත ක්රම අයත් වේ: නැවුණු ප්රෝටීනවලට ආධාර කරන සහ නොනැවුණු ප්රෝටීන ඉවත් කරන චැපරෝන් ප්රෝටීනවලට බලපෑම් ඇති කිරීම; සෛල ඉවත් කිරීමේ ක්රියාවලියට ආධාර වන කැස්පේස් එන්සයිම සමග අන්තර්ක්රියා කිරීම; ස්නායු සෛල මත ග්ලූටැමීන් නිසා ඇති වන ධූලක ක්රියා; සෛලය තුළ ශක්තිය නිපදවීම අඩු කිරීම; සහ ජාන ප්රකාශ වීමට බාධා පැමිණවීම වැනි තත්ත්ව එසේ හඳුනාගෙන ඇත.[39][40]
හන්ටිංටන් රෝගයේ දී සෛලීය කෘත්යයන් අඩාල වන තවත් ආකාරයක් විස්තර කෙරෙන වාදයක් ඇත. මෙහි දී යෝජනා වී ඇත්තේ striatal සෛලවල මයිටොකොන්ඩ්රියාවලට හානි සිදුවන බවයි. (මයිටොකොන්ඩ්රීය පරිවෘත්ති ඌනතා රාශියක් පිළිබඳ වාර්තා හමුවේ) එසේම විකල්ප හන්ටිංටින් ප්රෝටීනය සහ නියුරෝනවල ඇති නොයෙකුත් ප්රෝටීන අතර ඇතිවන අන්තර්ක්රියා හේතුවෙන් ග්ලූටැමීන්හි අවදානම් තත්ත්වය ඉහළ යන අතර, එය විශාල ප්රමාණවලින් පවතින විට බහිඃසෛලීය ධූලකයක් ලෙස ක්රියා කරයි. මෙම ධූලක නොයෙකුත් සෛලීය ව්යූහයන්ට හානි සිදු කරයි. ග්ලූටැමීන් අතිවිශාල ප්රමාණවලින් හමුනොවූව ද, ඒවායේ අවදානම්කාරී ස්වභාවය වැඩි නිසා සාමාන්ය ග්ලූටැමීන් ප්රමාණ පවා බහිඃසෛලීය ධූලක ලෙස ක්රියා කරතැයි උපකල්පනය කෙරේ.[39]
මහේක්ෂීය වෙනස්කම්
[සංස්කරණය]
හන්ටිංටන්ගේ රෝගය නිසා සම්පූර්ණ මොළයටම බලපෑම් ඇති වුව ද, සෙසු ස්ථානවලට වඩා බෙහෙවින් බලපෑමට ලක්වන ස්ථාන කිහිපයක් පවතියි. මින් වඩාත් ප්රමුඛ මුල්කාලීන බලපෑම් ඇතිවන ස්ථානය පාදීය ගැංග්ලියාවල කොටසක් වන neostriatum ප්රදේශයයි. මෙය සපුච්ඡ න්යෂ්ටිය සහ putamen යන පෙදස්වලින් සමන්විත ය.[23] බලපෑම් ඇතිවන සෙසු ස්ථාන අතරට substantia nigra, අනුමස්තිෂ්ක බාහිකයේ 3, 5 සහ 6වන ස්තර, හිපොකැම්පසය, අනුමස්තිෂ්කයේ පර්කින්ජි සෛල, හයිපොතැලමසේ පාර්ශ්වික ප්රාර්බුද න්යෂ්ටි සහ තැලමසේ කොටසක් අයත් වේ.[24] මෙම ප්රදේශ බලපෑමට ලක්වන්නේ ඒවායේ ව්යූහය සහ එහි අන්තර්ගත නියුරෝන වර්ග අනුව ය.[24] මින් striatum ප්රදේශයේ පිහිටි සකණ්ඨක නියුරෝන වඩාත් අවදානමට ලක්වේ. ප්රධාන වශයෙන්ම බාහිර globus pallidus දෙසට පිහිටි නෙරුම් සහ අභ්යන්තර pallidum පෙදෙස වෙත නෙරා ඇති අන්තරනියුරෝන සහ සකණ්ඨක සෛල අවදානමට ලක්වන්නේ අඩුවෙනි.[24][41] මීට අමතරව හන්ටිංටන්ගේ රෝගය නිසා ඇස්ට්රොසයිට සංඛ්යාව අසාමාන්ය වැඩිවීම සහ මොළයේ ප්රතිශක්ති සෛලවන මයික්රොග්ලියා ක්රියාකාරී වීම ද සිදුවේ.[42]
මුල්කාලීනව හන්ටිංටන්ගේ රෝගයෙන් වඩාත් බලපෑමට ලක්වන පාදීය ගැංග්ලියා, චලන සහ හැසිරීම් පාලනයේ දී වැදගත් කාර්යභාරයක් ඉටු කරයි. ඒවායේ කෘත්යය මෙතෙක් සම්පූර්ණයෙන් වටහාගෙන නැත. නමුත් පවතින මතයන් අනුව, ඒවා ඥානාත්මක කාරක පද්ධතිය (executive system)[17] සහ චාලක පරිපථය හා සම්බන්ධ යැයි සිතිය හැක.[43] සාමාන්යයෙන් පාදීය ගැංග්ලියා මගින්, විශේෂිත චලන ඇතිකරන ස්නායු පථ රැසක් නිෂේධනය කරයි. නිශ්චිත චලනයක් ඇරඹීම සඳහා මස්තිෂ්ක බාහිකය මගින් පාදීය ගැංග්ලියා වෙත යැවෙන සංඥා අනුව එම පථයන් නිෂේධනය කිරීම හෝ නිදහස් කිරීම සිදුවේ. පාදීය ගැංග්ලියාවලට හානි සිදුවීමෙන් ඒවායේ නිෂේධන මුදාහැරීම හෝ පිහිටුවීම පාලනය රකගත නොහැකි වේ. මේ නිසා අනභිප්රායික චලනයක් අසාමාන්ය ලෙස ඇරඹීම, චලනයක් එහි කාර්යය සම්පූර්ණ වීමට පෙර හෝ කාර්යය සම්පූර්ණ කර වේලාවකට පසුව නැවතීම වැනි තත්ත්ව ඇතිවිය හැක. මෙම ප්රදේශයට දිගින් දිගටම සිදුවන හානිය නිසා හන්ටිංටන් රෝගය හා සම්බන්ධ ලාක්ෂණික අස්ථිර චලන ඇතිවේ.[43] හන්ටිංටන්ගේ රෝගය හා සම්බන්ධ නිරායාස හා අස්ථිර කායික චලනයන් අතිගතිචාර දුෂ්පාර්වයේ (hyperkinetic dysarthria) එක් ප්රභේදයක් ලෙස වර්ගීකරණය කොට ඇත. චලන නිෂේධනයට පාදීය ගැංග්ලියාවලට නොහැකි වීමෙන්, රෝගයෙන් පෙළෙන්නන්හට කථන අපහසුතාවන් සහ ආහාරපාන ගිලීමේ අපහසුතා ඇතිවේ.[44]
ප්රතිලේඛන දුර්නියාමනය
[සංස්කරණය]CREB-බන්ධක ප්රෝටීනය (CBP) නැමැති ප්රතිලේඛන සහ-යාමකය සෛලීය ක්රියාකාරීත්වය සඳහා අත්යාවශ්ය වන්නේ එමගින් ප්රෝටීන සංස්ලේෂණයේ දී ජාන ප්රතිලේඛනය ප්රවර්තන මාර්ග ඔස්සේ සක්රීය කරන නිසායි.[45] මීට අමතරව, CBP තැනීමට දායක වන ඇමයිනෝ අම්ල අතරට, අණු 18කින් යුත් ග්ලූටැමීන් දාමයක් ද ඇතුළත් වේ. මේ නිසා, CBPහි ඇති ග්ලූටැමීන ඍජුවම HTT ජානයේ ඇති සංඛ්යාවෙන් වැඩි වූ ග්ලූටැමීන සමග අන්තර්ක්රියා කරයි. මෙවිට, න්යෂ්ටියට යාබදව පිහිටි CBP එහි සාමාන්ය පිහිටුමෙන් ඉවතට තල්ලු වේ.[46] විශේෂයෙන්ම, CBPහි අන්තර්ගත වන ඇසිටයිල්ට්රාන්ස්ෆරේස් ප්රදේශයට HTT ජානය එහි පොලිග්ලූටැමීන්-අන්තර්ගත පෙදෙස මගින් බැඳීම සිදුවේ.[47] මරණ පරීක්ෂණවල දී, හන්ටිංටන් රෝගීන්ගේ මොළවල CBP ප්රමාණය අසාමාන්ය ලෙස අතිශය පහළ අගයයක් ගන්නා බව පෙනී ගොස් ඇත.[46] මීට අමතරව, CBP ප්රෝටීනය අතිශයින් ප්රකාශ වන විට, පොලිග්ලූටැමීන් හේතුවෙන් සිදුවන මරණ අවදානම අඩු වේ. එසේම සාමාන්යයෙන් CBP ප්රෝටීනය හන්ටිංටන් රෝගය ඇතිවීම සහ නියුරෝනවල ක්රියාකාරීත්වය කෙරෙහි වැදගත් වන බව පෙනීගොස් ඇත.[45]
රෝග විනිශ්චය
[සංස්කරණය]හන්ටිංටන් රෝගයේ ආරම්භක අවස්ථාවේ රෝග විනිශ්චය රෝගයට විශේෂිත වන කායික රෝග ලක්ෂණ අනුසාරයෙන් සිදුකළ හැක.[11] හන්ටිංටන් රෝගය පිළිබඳ පවුල් ඉතිහාසයක් නොමැති විට, ජාන පරීක්ෂාවක් මගින් කායික රෝග නිර්ණය සිදුකළ හැක. රෝග ලක්ෂණ ආරම්භ වීමටත් පෙර, ප්රවේණි පරීක්ෂාවක් මගින් පුද්ගලයකු හෝ කලලයක් සතුව, රෝගයට හේතුවන HTT ජානයේ ට්රයිනියුක්ලියෝටයිඩ පුනරාවර්තනයේ ප්රසාරිත පිටපතක් තිබේදැයි නිර්ණය කරගත හැක. පරීක්ෂා ක්රියාවලියේ දී සහ සනාථ කරගත් පසුව ප්රවේණි උපදේශනය මගින් උපදෙස් සැපයීම සහ මගපෙන්වීම සිදුකෙරේ. මෙහි දී, පුද්ගලයාගේ මානසික තත්ත්වය, රැකියාව, පවුල් සැලසුම් තීරණ, ඥාතීන් සහ ඥාති සබඳතා පිළිබඳ අවධානය යොමු කෙරේ. රෝග ලක්ෂණ මතුවීමට පෙර කළ හැකි පරීක්ෂා ද පැවතුණත්, ඒ කෙරෙහි යොමුවන්නේ හන්ටිංටන්ගේ රෝගය උරුමවන්නන්ගෙන් 5%ක පමණ සුළු පිරිසකි.[23]
සායනික
[සංස්කරණය]
රෝගයේ ආරම්භය හඳුනා ගැනීමට කායික පරීක්ෂණයක් මෙන්ම ඇතැම්විට ඒ හා සංයුක්තව මනෝවෛද්ය පරීක්ෂණයක් ද සිදුකරනු ලබයි.[11] සිරුරේ ඕනෑම කොටසක ඇතිවිය හැකි අනභිප්රායික චලන නිසා පුද්ගලයින් බොහෝ අවස්ථාවල දී වෛද්ය උපදේශන ලබා ගැනීමට පෙළඹේ. මේවා හදිසියේම එහෙත්, අහඹු වශයෙන් සිදුවන්නේ නම් වෛද්යවරුන් විසින් හන්ටිංටන්ගේ රෝගය සඳහා පරීක්ෂණය කළ යුතු බවට නිර්දේශ කරනු ලබයි. ඥානාත්මක හෝ චර්යාත්මක රෝග ලක්ෂණ මුලින් හඳුනාගන්නා අවස්ථා විරළ ය. මේවා බොහෝ විට හඳුනාගත හැකි වන්නේ රෝගය තවදුරටත් වර්ධනය වූ විටයි. රෝගය කෙතරම් දුරට වර්ධනය වී ඇත්ද යන්න මැන ගැනීමට ඒකාබද්ධ හන්ටිංටන්ගේ රෝග ප්රමාණන පරිමාණය භාවිතා කළ හැක. මෙම පරිමාණය මගින් චාලක, චර්යාත්මක, ඥානාත්මක සහ කෘත්යමය තක්සේරුවක් සිදුකොට සිරුර පිළිබඳ සමස්ත ඇගයුමක් ලබා දේ.[49][50] පරිගණකගත තීරු ප්රතිබිම්බකරණය (CT) සහ චුම්බක අනුනාද ප්රතිබිම්බකරණය (MRI) වැනි වෛද්ය විද්යාත්මක පරිලෝකන ක්රම මගින් රෝගයේ මුල්කාලීන අවස්ථාවේ දී, දකුණු පස රූපයේ දක්වා ඇති පරිදි සපුච්ඡ න්යෂ්ටිවල ක්ෂීණවීම නිරීක්ෂණය කළ හැක. නමුත් මෙම වෙනස්වීම් හන්ටිංටන් රෝගය නිසාම ඇති නොවන අවස්ථා ඇත. රෝගයේ වැඩිදියුණු අවස්ථාවල මස්තිෂ්ක ක්ෂය වීම දැකගත හැක. කෘත්යමය චුම්බක අනුනාද ප්රතිබිම්බකරණය (fMRI) සහ පොසිට්රෝන විමෝචන තීරු ප්රතිබිම්බකරණය (PET) වැනි කෘත්යමය ස්නායුප්රතිබිම්බකරණ ක්රමවේද අනුසාරයෙන් භෞතික රෝග ලක්ෂණ මතුවීමට පෙර මොළයේ වෙනස්වීම් හඳුනාගත හැක. නමුත් මේවා පර්යේෂණාත්මක උපකරණ හෙයින්, සායනික කටයුතුවල දී භාවිතා නොවේ.[24]
පුරෝකථන ජාන පරීක්ෂා
[සංස්කරණය]හන්ටිංටන්ගේ රෝගය අලිංග වර්ණදේහ ප්රමුඛ ආවේණි රටාවක් සහිත බැවින්, එය උරුමවීමේ අවදානම සහිත පුද්ගලයින් පරීක්ෂාවලට සහභාගී වීම අත්යාවශ්ය ය. හන්ටිංටන්ගේ රෝගය සඳහා ප්රවේණි පරීක්ෂාවක් සිදු කිරීමේ දී රුධිර පරීක්ෂාවක් මගින් සෑම HTT ඇලීලයකම පවතින CAG පුනරාවර්තන සංඛ්යාව ගිණීම සිදු කෙරේ.[51] මෙහි කඩඉම් අගයයන් පහත දැක්වේ:
- CAG පුනරාවර්තන ඒකක 40ක් හෝ ඊට වඩා පිහිටීම: සම්පූර්ණයෙන් නිවේධනය වන (penetrance) ඇලීලයකි (FPA).[52] "ධන පරීක්ෂාව"ක් හෝ "ධන ප්රතිඵලයක්" මෙම අවස්ථාව හා අදාළ වේ. ධන ප්රතිඵලයක් රෝග විනිශ්චයක් ලෙස නොසැලකේ. එයට හේතුව රෝග ලක්ෂණ ඇරඹීමට දශකයකට පමණ පෙර මෙය හඳුනාගත හැකි වීමයි. කෙසේනමුත්, ඍණ පරීක්ෂාවක් යන්නෙන් හෙළිවන්නේ එම පුද්ගලයා සතුව ජානයේ ප්රසාරිත පිටපත් නොමැති බවත්, ඔහු තුළ හන්ටිංටන්ගේ රෝගය වර්ධනය නොවන බවත් ය.[24] මෙම පරීක්ෂාව මගින් රෝගය උරුමවීමේ සියයට 50ක සම්භාවිතාවක් සහිත පුද්ගලයකුට, එහි අවදානම සියයට 100 තෙක් ඉහළ යයි ද නැතහොත් අවදානමක් නොමැති ද යන්න දැනගත හැක. මෙම පරීක්ෂාවෙන් ධන ප්රතිඵලයක් ලැබෙන පුද්ගලයින්ගේ ජීවිත කාලයේ කුමන හෝ අවස්ථාවක හන්ටිංටන්ගේ රෝගය වර්ධනය විය හැක.[24]
- පුනරාවර්තන 36 සිට 39 දක්වා: අසම්පූර්ණ හෝ ඌන නිවේධිත ඇලීලයකි (RPA). මෙහි දී ඇතැම්විට වැඩිහිටි වියේ පසු කාලයක දී රෝග ලක්ෂණ ඇතිවිය හැක.[52] RPA සහිත පුද්ගලයකුට 65වන වියේ දී රෝග ලක්ෂන පහළ වීමට 60%ක අවදානමක් ඇත. එසේම 75වන වියේ දී රෝග ලක්ෂණ පහළ වීමේ 70%ක අවදානමක් ඇත.[52]
- පුනරාවර්තන 27 සිට 35 දක්වා: අන්තර්මධ්ය ඇලීලය (IA), හෝ විශාල සාමාන්ය ඇලීලය. මෙය පරීක්ෂා කළ පුද්ගලයාගේ රෝග ලක්ෂණ හා සම්බන්ධ නොවේ. නමුත් ඔහුගේ ඉදිරි පරම්පරාවලට උරුමවීමේ වැඩිදුර හැකියාව පිළිබඳ සොයා බැලේ.[52]
- පුනරාවර්තන 26 හෝ ඊට වඩා අඩු: හන්ටිංටන්ගේ රෝගය හා සම්බන්ධයක් නැත.[52]
පූර්ව-රෝග ලක්ෂණික පරීක්ෂාවක් යනු දිවිය වෙනස් කිරීමට හේතුවන අතිශය පෞද්ගලික තීරණයකි.[24] හන්ටිංටන්ගේ රෝගය සඳහා පරීක්ෂා සිදු කිරීමෙන් ඔවුන්ගේ වෘත්තීන්ට ආධාර වීම සහ පවුල් තීරණවලට සහාය දැක්වීම සිදු කළ හැක.[24] 1993ට පෙර, තමන් හන්ටිංටන්ගේ ජානය දරන්නකුදැයි හඳුනා ගැනීමට නිශ්චිත පරීක්ෂා නොතිබිණි. එකල පර්යේෂණ මගින් අනාවරණය වූයේ පුරෝකථන පරීක්ෂාවන් සිදු කළේ සුළු පිරිසක් සඳහා වුව ද, අවදානම් සහිත පුද්ගලයින්ගෙන් 50–70% පමණ පරීක්ෂා කරගැනීමට අදහස් කළ බවයි.[53] මේ සඳහා නිශ්චිත ප්රතිකාරයක් නොමැති හෙයින් හන්ටිංටන්ගේ රෝගය උරුමවීමේ අවදානම සහිත පුද්ගලයින්ගෙන් 95%ක් පමණම පරීක්ෂා සිදු කරගැනීමට නොපෙළඹේ.[24] ධන ප්රතිඵල හා සැසඳීමේ දී තමන් තුළ හන්ටිංටන්ගේ රෝගය ක්රමයෙන් වර්ධනය වේ යැයි දැන නොසිටීම නිසා පුද්ගලයින් තුළ සාංකාවක් ඇති විය හැක.[23] ප්රතිඵලය සැලකිල්ලට නොගත් විට, පරීක්ෂාවට ලක්කොට වර්ෂ දෙකකට පසු පුද්ගලයාගේ ආතති මට්ටම පහත වැටී ඇති බව දක්නට ලැබී ඇත. නමුත් පරීක්ෂාවේ දී ධන ප්රතිඵලයක් ලැබුණු විට පුද්ගලයාගේ සියදිවි නසා ගැනීමේ ප්රවණතාව ක්රමයෙන් වැඩි වී ඇති බව පෙනේ.[23] රෝගී සාමාජිකයන් සිටින පවුලක, ආබාධය උරුම නොවූ බව අනාවරණය කරගත් පුද්ගලයින්ට නොනැසී සිටීම පිළිබඳ සාපරාධී හැඟීමක් (survivor guilt) ජනිත විය හැක.[23] මෙහි දී සැලකිල්ලට ගත් තවත් කරුණක් වන්නේ, පරීක්ෂාවක දී ධන ප්රතිඵලයක් හිමිවූ විට අදාළ පුද්ගලයාගේ දෙමාපියකු සතුව විකෘති ජානය සහිත බව හැඟවෙන බැවින්, එම පුද්ගලයාගේ සහෝදර/සහෝදරියන්ට ද එම ආබාධය උරුමවීමේ අවදානමක් සහිත වීමයි.[23] එක්තරා අධ්යයනයක දී, හන්ටිංටන්ගේ රෝගය සඳහා අවදානමක් ඇති පුද්ගලයින්ගේ ප්රවේණි විචක්ෂණය (genetic discrimination) 46%ක් බව හෙළි විය. මෙය සෞඛ්යාරක්ෂණ හෝ වෘත්තීයමය සබඳතාවලට වඩා පෞද්ගලික සබඳතා කෙරෙහි වැඩිපුර බලපෑවේ ය.[54] හන්ටිංටන් රෝගය සඳහා ප්රවේණි උපදේශනය මගින් පරීක්ෂා ක්රියාවලියේ සෑම පියවරක දී ම, අවශ්ය තොරතුරු දැන ගැනීම, තීරණ ගැනීමේ දී උපදෙස් හා සහාය ලබා දීම සිදු කෙරේ.[55] මෙම පරීක්ෂාවේ ඇති සංකීර්ණභාවය නිසා පරීක්ෂාවට ලක්වන්නට අපේක්ෂිත රෝගීන් හට හන්ටිංටන්ගේ රෝගය පිළිබඳ දැනුම්වත් කෙරෙන උපදේශන සැසි තුනක් පවත්වනු ලැබේ.[56]
හන්ටිංටන්ගේ රෝගය සඳහා ප්රවේණි පරීක්ෂාවේ දී සිදුකෙරෙන උපදේශන සහ මාර්ගසූචක අලිංග වර්ණදේහ ප්රමුඛ අනුමස්තිෂ්ක අනන්වය වැනි ප්රවේණි ආබාධ හඳුනා ගැනීමේ දී ද භාවිතා වේ.[23][57][58] හන්ටිංටන්ගේ රෝගය සඳහා සිදුකෙරෙන පූර්වරෝග ලක්ෂණික පරීක්ෂා කෙරෙහි පොලිසිස්ටික වෘක්ක රෝගය, කුටුම්භීය ඇල්ෂයිමර්ගේ රෝගය සහ පියයුරු පිළිකා වැනි ප්රවේණි ප්රභේදන සහිත වෙනත් රෝගවල පරීක්ෂා ද අදාළ කරගත හැක.[57] යුරෝපීය අණුක ප්රවේණිවිද්යා තත්ත්ව ජාලය විසින් මෙම රෝගයේ අණුක ප්රවේණි පරීක්ෂාවන් සඳහා වාර්ෂික බාහිර තත්ත්ව තක්සේරු නිර්ණායක හඳුන්වා දී ඇත. මේ නිසා හන්ටිංටන්ගේ රෝගයේ ප්රවේණි පරීක්ෂා සඳහා හොඳම ප්රායෝගික ක්රමවේදයන් සහ ප්රතිඵල වාර්තා කරන අයුරු පිළිබඳ මාර්ගෝපදේශයක් ලබාගත හැක.[59]
පූර්ව-අධිරෝපණ ප්රවේණි රෝග විනිශ්චය
[සංස්කරණය]බාහිරව සංසේචනය කරන ලද කලල, පූර්වඅධිරෝපණ ප්රවේණි රෝග විනිශ්චය (PGD) ආධාර කරගනිමින් හන්ටිංටන්ගේ රෝගය සඳහා පරීක්ෂා කෙරේ. මෙම ක්රමවේදයේ දී, සාමාන්යයෙන් සෛල 4 සිට 8 දක්වා සංඛ්යාවකින් යුතු කලලයෙන් සෛල එකක් හෝ දෙකක් ලබාගෙන එහි ප්රවේණි අසාමාන්යතා ඇත්දැයි පරීක්ෂා කෙරේ. එමගින් හන්ටිංටන්ගේ රෝගය හේතුවීමට අදාළ ජානය සහිත කලල අධිරෝපණය වළක්වා ගත හැක. මෙවිට කිසිදු ජනිතයකුට රෝගය උරුම නොවේ. අනාවරණ-නොවන හෝ නිෂේධන පරීක්ෂා වැනි ඇතැම් පූර්ව-අධිරෝපණ ප්රවේණි පරීක්ෂා මගින් අවදානම් සහිත පුද්ගලයින්ට හන්ටිංටන්ගේ රෝගයෙන් තොර ජනිතයින් ලබාගත හැක. මෙහි දී ඔවුන්ගේ ජනක ප්රවේණිදර්ශය අනාවරණය නොකෙරෙන අතර, ඔවුනට හන්ටිංටන්ගේ රෝගය ඇතිවේදැයි තොරතුරු නොසපයනු ලැබේ. නිෂේධන පරීක්ෂාවක දී, කලලයේ DNA, දෙමාපියන්ගේ සහ ඔවුන්ගේ පූර්වජනකයින්ගේ DNA සමග සසඳා පූර්වජනකයින්ගෙන් හන්ටිංටන්ගේ රෝගයේ ජානය සහිත වර්ණදේහ පෙදෙස උරුමවීම වළකනු ලැබේ. අනාවරණ-නොවන පරීක්ෂාවක දී, රෝගය නොමැති කලල පමණක් ගර්භාෂය තුළ තැන්පත් කෙරේ. මේ නිසා ජනක ප්රවේණිදර්ශය සහ හන්ටිංටන්ගේ රෝගය සඳහා දෙමාපියන් තුළ ඇති අවදානම කිසිදින අනාවරණය නොවේ.[60][61]
පුරඃප්රසව පරීක්ෂා
[සංස්කරණය]ගර්භාෂය තුළ සිටින කලලයක් හෝ භ්රෑණයක් සඳහා ද පුරඃප්රසව රෝග විනිශ්චයක් සිදුකළ හැක. මෙහි දී කෝරියම් අංගුලිකා නියැදි ආධාරයෙන් භ්රෑණයේ ප්රවේණි ද්රව්ය ලබා ගැනේ. ගර්භනීභාවය වඩා දීර්ඝ නම් සති 14-18 ඇතුළත ඇම්නියෝසෙන්ටෙසිස් (amniocentesis) ක්රමවේදය අනුගමනය කළ හැක. මෙහි දී දරුවා වටා ඇති කලලාවාරික තරලයේ හන්ටිංටන්ගේ රෝගයේ විකෘතිය සහිත දැයි පරීක්ෂා කෙරේ.[62] මෙය ද දෙමාපිය ප්රවේණිදර්ශය අනාවරණය වීම වැළැක්වීමට නිෂේධ පරීක්ෂාවක් සමග සිදුකළ හැක. දෙමාපියකු තුළ හන්ටිංටන්ගේ රෝගය ඇතිබව විනිශ්චය කළ පසුව, පුරඃප්රසව පරීක්ෂාව සිදුකළ හැක. මෙය විශේෂයෙන්ම ජාන පරීක්ෂාවේ දී HTT ජානයේ ප්රසාරණයක් හෝ උරුමවීමේ 50%ක අවදානමක් ඇති විට සිදුකරනු ලැබේ. දෙමාපියන්හට විකල්ප ක්රම පිළිබඳ උපදේශන යෝජනා කෙරේ. මෙයට ගැබ්කාලය අවසන් කිරීම, සහ හඳුනාගත් ජානය සහිත දරුවකුගේ ආබාධ ඇතුළත් වේ.[63][64]
මීට අමතරව, රෝගී පුරුෂ සහකරුවකු නිසා ඇතිවන අවදානම් සහගත ගර්භනීභාවයන්හි දී, ආක්රමණික-නොවන පුරඃප්රසව රෝග විනිශ්චය (non-invasive prenatal diagnosis) භාවිතා කළ හැක. මෙහි දී ගර්භනීභාවයේ සයවන සහ දොළොස්වන සති අතර කාලයේ මවගෙන් ලබාගත් රුධිර සාම්පලයක සෛල-නිදහස් භ්රෑණ DNA පරීක්ෂා කෙරේ.[52] මෙම ක්රියාවලිය සතුව ක්රියාවලි-ආශ්රිත ගබ්සා අවදානමක් නොමැත. (ඉඳිකටු ආසාදනයක් ඔස්සේ හැර)[52]
ආන්තර රෝග විනිශ්චය
[සංස්කරණය]හන්ටිංටන්ගේ රෝගයේ රෝග විනිශ්චය 99%ක් පමණම පාදක වී ඇත්තේ දර්ශීය රෝග ලක්ෂණ සහ රෝගය සඳහා වන පවුල් ඉතිහාසය මත ය. මෙය හන්ටිංටන්ගේ රෝගයට හේතු වන ප්රසාරිත ට්රයිනියුක්ලියෝටයිඩ පුනරාවර්තනය පිළිබඳ ප්රවේණි පරීක්ෂාවකින් සිදුකළ හැක. සෙසු ආකාර බොහෝමයක් HD-වැනි (HDL) සහලක්ෂණ ලෙස හඳුන්වයි.[16][65] බොහෝ HDL රෝග සඳහා හේතූන් නොදනී. නමුත් හේතූන් හඳුනාගත් ඇතැම් රෝග ප්රියෝන ප්රෝටීන ජානය (HDL1), ජන්ක්ටොෆිලින් 3 ජානය (HDL2), නිලීනව උරුම වන නොදන්නා ජානයක් (HDL3—පවුල් ආකාර දෙකක පමණක් හමුවේ. වටහාගෙන ඇත්තේ මඳ වශයෙනි), සහ TATA කොටු-බන්ධ ප්රෝටීනයේ කේතන ජානය (SCA17, හෙවත් HDL4) යන ජානවල ඇතිවන විකෘති නිසා ඇතිවේ. හන්ටිංටන්ගේ රෝගය ලෙස වරදවා වටහාගත හැකි සෙසු අලිංග වර්ණදේහ ප්රමුඛ රෝග අතරට dentatorubral-pallidoluysian atrophy සහ neuroferritinopathy වැනි රෝග ඇතුළත් විය. මීට අමතරව හන්ටිංටන්ගේ රෝගයට සමානත්වයක් දක්වන විරළ අලිංග වර්ණදේහ නිලීන ආබාධ ද ඇත. මේ අතරට, කෝරියා ඇකැන්තොසයිටෝසිස් සහ පැන්ටොතෙනික් කයිනේස්-සම්බන්ධ ස්නායුපරිහානිය වැනි ආබාධ අයත් ය. මෙම ආකාරයේ එක් X-ප්රතිබද්ධ ආබාධයක් නම් මැක්ලියොඩ් සහලක්ෂණයයි.[65]
කළමනාකරණය
[සංස්කරණය]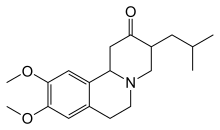
හන්ටිංටන්ගේ රෝගයට ප්රතිකර්ම නොමැත. නමුත් එහි ඇතැම් රෝග ලක්ෂණ පාලනයට විවිධ ප්රතිකාර ක්රම අනුගමනය කෙරේ.[66] මෙම ප්රතිකාර ක්රම රැසක, හන්ටිංටන්ගේ රෝගයේ රෝග ලක්ෂණවලට ප්රතිකාර කිරීමේ සඵලතාව සනාථ කිරීමට සාක්ෂි අසම්පූර්ණ ය.[67][68] රෝගය වර්ධනය වත්ම, යම් පුද්ගලයකුට තමන්ව රැකබලා ගැනීමේ හැකියාව අවම වන අතර, ඔවුන්ව රැකබලාගැනීමේ අවශ්යතාව වැඩි වේ.[67] සාපේක්ෂව සුළු අධ්යයන සහ චිකිත්සක ක්රම ප්රමාණයක් මගින් හන්ටිංටන්ගේ රෝගයේ ඥානාත්මක රෝගලක්ෂණ පුනරුත්ථාපනයට උපකාරී වන බව සොයාගෙන ඇත. එහිදී භෞතික චිකිත්සාව, වෘත්තීය චිකිත්සාව, සහ කථන චිකිත්සාව වැනි චිකිත්සක ක්රම වැදගත් වේ.[11] හන්ටිංටන්ගේ රෝගය මුල් වයස්වලදී ඉස්මතු වීම සහ කැෆේන් භාවිතය අතර යම් සම්බන්ධතාවක් ඇති බැව් පෙනීගොස් ඇත.[69][70] නමුත් මෙම සොයාගැනීම අතීතාවර්ජන ප්රශ්නාවලියක් අනුසාරයෙන් පාදක වී ඇති නිසා, ජීවන රටාව පිළිබඳ තීරණ ගැනීමට මෙය උපකාර කරගත හැක්කේ මඳ වශයෙනි.[71]
භෞතීය චිකිත්සාව
[සංස්කරණය]දුර්භක්ෂ (dysphagia) ඇතුළු සෙසු පේශී සමායෝජන දුර්වලතා හේතුවෙන් දේහ බර අඩු වීම සහ ආහාර ගැනීමේ අපහසුතා ඇතිවේ. මේ නිසා රෝගය වර්ධනය වනවිට පෝෂණ කළමනාකරණය අතිශයින් වැදගත් වේ.[67] උකු ද්රව ගිලීමට පහසු හෙයින් ද්රව ආහාරවලට ඝනීකාරක එකතු කොට ආහාරයට ගත හැක.[67] රෝගී පුද්ගලයාට සෙමෙන් ආහාර ගැනීමට සහ ආහාර කුඩා කැබලි ලෙස ආහාරයට ගැනීමට සිහිපත් කරවීමෙන් ආහාර හිරවීම වළක්වා ගත හැක.[67] ආහාර ගැනීමට උපද්රවකාරී හෝ ඉතා අපහසු නම්, සම තුළින් යෙදෙන ආමාශ ඡේදක එන්ඩොස්කෝපයක් (percutaneous endoscopic gastrostomy) භාවිතා කළ හැක. මෙය උදරය ඔස්සේ ආමාශය තුළට ස්ථිරව සම්බන්ධ කළ පෝෂණ නළයකි. මෙමගින් ආහාර ශ්වසන මාර්ගයට ඇතුළු වීමේ අවදානම අඩුවී මනා පෝෂණ කළමනාකරණයක් පවත්වා ගත හැක.[72] කථන සහ භාෂා චිකිත්සකවරුන්ගේ සහාය ආධාරයෙන් කළමනාකරණය කිරීම හන්ටිංටන්ගේ රෝගය සඳහා නිර්දේශ කෙරේ.[11]
හන්ටිංටන්ගේ රෝගය සහිත පුද්ගලයින්හට කායික රෝගලක්ෂණ පාලනයට භෞතීය චිකිත්සකවරයකු හමුවී ආක්රමණික-නොවන සහ ඖෂධ-පාදක කරනොගත් ක්රමවේද උපයෝගී කරගත හැක. භෞත චිකිත්සකවරුන් අවදානම පහත හෙළීමේ සහ වැළැක්වීමේ ක්රමවේද මෙන්ම ශක්තිමත් කිරීම, ඇදීමේ සහ හෘත් සනාල ව්යායාම පුහුණු කරවනු ලැබේ. ඇවිදීමේ ආධාර ද ඇතැම්විට සුදුසු යැයි සැලකේ. ශ්වසන ආබාධ මඟහැරවීම සඳහා භෞත චිකිත්සකවරුන් විසින් ශ්වසන අභ්යාස සහ වාමඟ පවිත්ර කිරීමේ ක්රමවේද නිර්දේශ කරනු ලබයි.[73] හන්ටිංටන්ගේ රෝගය පිළිබඳ භෞතීය චිකිත්සා සම්මුතික නිර්දේශයන් නිර්මාණය කරන ලද්දේ යුරාපීය HD ජාලය විසිනි.[73] මුල්කාලීන පුනරුත්ථාපන අර්ථකථනයන්ගේ අරමුණ කෘත්යයන් අඩාල වීම වැළැක්වීමයි. රෝගයේ මුල්කාලීන සිට මධ්යම දක්වා වූ අවධිවල රෝගීන්හට මෙම පුනරුත්ථාපන වැඩසටහන්වලට සහභාගී වීම වාසිදායක වන්නේ එමගින් දිගුකාලීන චාලක සහ කෘත්යමය ක්රියාකාරීත්වයන් පවත්වාගැනීමට ආධාර වන නිසායි. පසුකාලීන අවධියේ පුනරුත්ථාපන ක්රියාවලි මගින් චාලක සහ කෘත්යමය හානි පූරණය කිරීමට උත්සාහ දරනු ලැබේ.[74] දිගුකාලීන ස්වාධීන කළමනාකරණය සඳහා, චිකිත්සකවරුන් විසින් සුදුසු පුද්ගලයින්ට ගෘහාශ්රිත ව්යායාම නිර්දේශ කරනු ලැබේ.[75]
ඖෂධ භාවිතය
[සංස්කරණය]එක්සත් ජනපදය තුළ 2008දී හන්ටිංටන්ගේ රෝගයේ කෝරියා තත්ත්වයට ප්රතිකාර කිරීමට ටෙට්රාබෙනැසයින් අනුමත කෙරිණි.[76] කෝරියාව පහත හෙළීමට උපකාරී වන සෙසු ඖෂධ අතරට නියුරොලෙප්ටිකයන් සහ බෙන්සොඩයසෙපීන ඇතුළත් වේ.[12] ඇමන්ටැඩින් හෝ රිමැසිමයිඩ් වැනි සංකීර්ණ තවමත් පර්යේෂණ මට්ටමේ පවතින නමුත්, ඒවා ද මූලිකව ධන ප්රතිඵල පෙන්වා ඇත.[77] විශේෂයෙන්ම බාලක අවධියේ ඇතිවන අවචාලකතාව (hypokinesia) සහ දෘඪභාවය සඳහා ප්රතිපාර්කින්සෝනියානු ඖෂධ භාවිතයෙන් ප්රතිකාර කළ හැකි අතර, myoclonic අතිචාලකතාව (hyperkinesia) සඳහා වැල්ප්රොයික් අම්ලය භාවිතා කරනු ලැබේ.[12]
මානසික රෝගලක්ෂණ සඳහා සාමාන්ය ජනයා සඳහා භාවිතා වන ඖෂධ භාවිතයෙන් ප්රතිකාර කළ හැක.[67][68] වරණීය සෙරටොනින් ප්රතිඅවබෝධ නිෂේධකය සහ මිර්ටසැපීන් යන ඖෂධ විෂාදය සඳහා නිර්දේශ කෙරේ. නමුත් අනාකෘතික ප්රතිසයිකෝසීය ඖෂධ නිර්දේශ කෙරෙන්නේ සයිකෝසීය සහ චර්යාත්මක ගැටලු සහිත රෝගීන් සඳහා පමණි.[68] දිගුකාලීන ප්රතිකාර අවශ්ය පුද්ගලයින් සඳහා බහුවිධ ඖෂධ සමග විශේෂඥ ස්නායුකමනෝවිද්යා ආදානයන් ද නිර්දේශ කෙරේ.[11]
අධ්යාපනය
[සංස්කරණය]හන්ටිංටන්ගේ රෝගය උරුමවූ හෝ උරුමවීමේ අවදානමක් සහිත පුද්ගලයින්ගේ පවුල්වලට හන්ටිංටන්ගේ රෝගය පිළිබඳ අත්දැකීම් ඇති නමුත් එය පිළිබඳ නිශ්චිත වැටහීමක් නොමැති වන්නට පුළුවන. විශේෂයෙන්ම මෑතකාලීන ප්රවේණි පරීක්ෂා, පවුල් සැලසුම් තේරීම්, ප්රතිකාර කළමනාකරණය සහ සෙසු කරුණු පිළිබඳ ඔවුනගේ අවබෝධය මඳ විය හැක. ප්රවේණි උපදේශනය මගින් මෙම පුද්ගලයන්ගේ දැනුම් යාවත්කාලීන කරමින්, වැරදි මතයන් දුරු කිරීමට ආධාරවන අතර, එය ඔවුන්ගේ අනාගත විසඳුම් සහ සැලසුම් නිර්මාණය කිරීමේ දී උපකාරී වේ.[23][78]
ප්රවේක්ෂණය (Prognosis)
[සංස්කරණය]ට්රයිනියුක්ලියෝටයිඩ පුනරාවර්තනයන්ගේ දිග, රෝග ලක්ෂණ ඇරඹීමේ වයස් විචලනයන් සහ ඒවා ක්රියාත්මක වන වේගය කෙරෙහි 60%ක් පමණම හේතු වේ. දිගින් වැඩි පුනරාවර්තන ඒකකයක් හේතුවෙන් මුල්කාලීන අවධියේ රෝගය ඉස්මතු වීම සහ රෝග ලක්ෂණ ශීඝ්රයෙන් ව්යාප්ත වීම සිදු වේ.[24][79] පුනරාවර්තන හැටකට අධික සංඛ්යාවක් සහිත පුද්ගලයින් තුළ වයස අවුරුදු 20 එළඹීමටත් පෙර රෝග ලක්ෂණ වර්ධනය වේ. එසේම ඒකක 40ට අඩු පුද්ගලයන් තුළ සැලකිය යුතු රෝග ලක්ෂණ කිසිදින වර්ධනය නොවේඅ.[80] සෙසු විචලනයන් පාරිසරික සාධක සහ රෝගයේ යන්ත්රණයට බලපාන සෙසු ජාන හේතුවෙන් ඇතිවේ.[24]
හන්ටිංටන් රෝගියකුගේ ආයු අපේක්ෂාව රෝග ලක්ෂණ ඉස්මතු වීමෙන් පසුව වර්ෂ 20ක් පමණ ය.[16] මොවුන්ගේ ජීවිතවලට වඩාත්ම තර්ජන එල්ල වන්නේ පේශී සමායෝජන දුර්වලතා හේතුවෙන් වන අතර, සුළු පිරිසකට ඥානාත්මක කෘත්යය පරිහානියට පත්වීම නිසා ඇතිවන චර්යාත්මක වෙනස්කම් ද හානිකර වේ. හන්ටිංටන් රෝගීන්ගේ මරණවලින් තුනෙන් එකක් පමණම සිදුවන්නේ නියුමෝනියාව හේතුවෙනි. චලන යාමනයට ඇති හැකියාව ක්රමයෙන් අඩු වන විට, පෙනහැලි පවිත්ර වීමේ හැකියාව දුර්වල වන අතර, ආහාර සහ පාන වර්ග ශ්වසන මාර්ගයට ඇතුළුවීමෙන් නියුමෝනියාව ඇතිවීමේ අවදානම ඉහළ යයි. දෙවන විශාලතම අවදානම වන්නේ හෘද රෝගයි. හන්ටිංටන් රෝගීන්ගේ මරණවලින් හතරෙන් එකක් පමණම මේ හේතුවෙන් සිදු වේ.[16] මරණ සඳහා හේතුවන තෙවන වඩාත් අවදානම් සහගත හේතුව සියදිවි නසාගැනීමයි. හන්ටිංටන් රෝගී මරණවලින් 7.3%ක් පමණම මේ නිසා සිදුවන අතර, රෝගීන් 27%ක් පමණ සියදිවි නසා ගැනීමට උත්සාහ දරා ඇත. චර්යාත්මක රෝග ලක්ෂණ, සියදිවි නසාගැනීමේ සිතිවිලි කෙරෙහි කුමන ප්රමාණයකින් බලපාන්නේ ද යන්න අපැහැදිළි ය. නමුත් රෝගීන්ට රෝගයේ පසුකාලීන අවධිවලින් පීඩා විඳීමට අපේක්ෂාවක් නොතිබීම මෙයට හේතු වේ.[81][82][83] සෙසු අවදානම් සාධක ලෙස අනුබාධනය (choking), වැටීමේන සිදුවන භෞතික තුවාල සහ මන්දපෝෂණය හඳුනාගෙන ඇත.[16]
වසංගතවේදය
[සංස්කරණය]හන්ටිංටන්ගේ රෝගය පසුකාලීන අවධියක දී ඇරඹීම මගින් හැඟවෙන්නේ එය සාමාන්යයෙන් ප්රජනනය කෙරෙහි බලනොපාන බවයි.[23] ලෝකය පුරා හන්ටිංටන්ගේ රෝග ව්යාප්තිය පුද්ගලයින් 100,000කට 5–10 පමණ ය.[84][85] නමුත් ජන වර්ගය, දේශීය සංක්රමණ සහ පසුගිය සංක්රමණ රටා හේතුවෙන් මෙය භූගෝලීය විචලනයක් පෙන්වයි.[23] මෙහි ව්යාප්තිය ස්ත්රීන් සහ පුරෂයන් අතර සමානව පවතී. බටහිර යුරෝපා සම්භවයක් ඇති පුද්ගලයින් තුළ මෙහි ව්යාප්තිය ඉහළ අතර, එය මිනිසුන් 100,000කට 7ක් පමණ වේ. ලෝකයේ සෙසු ප්රදේශවල එය පහත අගයයක් ගනියි. උදාහරණයක් වශයෙන් ආසියානු සහ අප්රිකානු සම්භවයක් ඇති පුද්ගලයින් තුළ එය මිලියනයකට එකක් පමණ වේ. 2013දී සිදුකරන ලද 1990 සහ 2010 අතර කාලය තුළ හන්ටිංටන්ගේ රෝග ව්යාප්තිය පිළිබඳ සිදුකළ වසංගත විද්යා සමීක්ෂණයකින් පෙනීගොස් ඇත්තේ එක්සත් රාජධානිය තුළ රෝගයේ ව්යාප්තිය 100,000කට 12.3ක් බවයි.[23][86] මීට අමතරව, කලාපීය ව්යාප්තියට සාපේක්ෂව එය තුළ පිහිටි ඇතැම් ප්රදේශ රෝගයේ ඉහළ ව්යාප්තියක් පෙන්වයි.[23] එවැනි ඉහළ අගයයක් වාර්තා වන ප්රදේශයකට උදාහරණයක් නම් වෙනිසියුලාවේ මැරකයිබෝ විල අවට වෙසෙන හුදකලා ජනගහනයයි. මෙහි හන්ටිංටන් රෝග ව්යාප්තිය පුද්ගලයින් 100,000කට 700ක් තරම් ඉහළ අගයයකි.[23][87] මෙවැනි ඉහළ ස්ථානීකරණ අගයයන් වාර්තා වන ප්රදේශ අතරට ටැස්මේනියාව හා ස්කොට්ලන්තයේ, වේල්සය සහ ස්වීඩනයේ විශේෂිත ප්රදේශ ඇතුළත් වේ.[83] ඇතැම් අවස්ථාවල මෙම ව්යාප්තිය ඉහළ යාමට භූගෝලීය හුදකලා ප්රදේශයක් වෙත සිදු වූ ඓතිහාසික සංක්රමණ හේතු විය හැක.[83][88] මින් ඇතැම් වාහකයින් වංශාවලි අධ්යයන මගින් වසර සිය ගණනක් පසුපසට හඳුනාගත හැක.[83] ප්රවේණි ඓකදර්ශයන් මගින් ද ව්යාප්තියේ භූගෝලීය ප්රභේදන සඳහා සාක්ෂි ලබා දේ.[83][89] මීට සාපේක්ෂව අයිස්ලන්තයේ තත්ත්වය තරමක් වෙනස් ය. ස්වීඩන්වරුන් මෙන්ම අයිස්ලන්තවරුන් ද, ස්කැන්ඩිනේවියාවේ මුල්කාලීන ජර්මන් ගෝත්රවලින් සම්භවය වුවත්, අයිස්ලන්තයේ හන්ටිංටන් රෝග ව්යාප්තිය පුද්ගලයින් 100,000කට 1කි.[90] ෆින්ලන්තය තුළ ද තරමක් පහළ අනුපාතයක් දක්නට ලැබෙන අතර එය පුද්ගලයින් 100,000කට 2.2කි.[91]
ප්රවේණි පරීක්ෂා හඳුන්වාදෙන තෙක්ම, සංඛ්යාලේඛන සඳහා භාවිතා වූයේ හන්ටිංටන්ගේ රෝගයේ කායික රෝග ලක්ෂණ හා පවුල් ඉතිහාසය පදනම් කරගත් සායනික රෝග විනිශ්චයයි. වර්තමානයේ ඉහත දත්ත පවා සංඛ්යාලේඛන යටතට ඇතුළත් කළ හැක. මින් වඩාත්ම සුලබ වී ඇත්තේ ප්රවේණි පරීක්ෂාවයි. මේ නිසා ආබාධයේ ව්යාප්තිය පිළිබඳ ඇස්තමේන්තු තරමක් ඉහළ යා හැකි බව පෙනේ.[83][92]
ඉතිහාසය
[සංස්කරණය]
හන්ටිංටන්ගේ රෝගය ආබාධයක් ලෙස මධ්යතන යුගයන්ගේ පවා හඳුනාගෙන තිබුණ ද, මෑතක් වනතුරුම එයට හේතුව වටහාගෙන තිබුණේ නැත. රෝගය පිළිබඳ වටහාගැනීම වෙනස්වීමත් සමග ඉතිහාසය පුරා හන්ටිංටන්ගේ රෝගයට විවිධ නම් ලබා දී ඇත. රෝගය හා සම්බන්ධ අචේතනික නර්තනාකාර චලන හේතුවෙන් මෙය මුලින් සරලව 'කෝරියාව' ලෙස හැඳින්විණි. මීට අමතරව හන්ටිංටන්ගේ රෝගය "ආවේණි කෝරියාව" සහ "නිධන්ගත ප්රගම්ය කෝරියාව" යන නම්වලින් ද හඳුන්වා ඇත.[94] හන්ටිංටන්ගේ රෝගය පිළිබඳ පළමු නිශ්චිත සඳහන හමුවන්නේ චාල්ස් ඔස්කාර් වෝටර්ස්ගේ ලිපියකිනිත මෙය 1842දී රොබ්ලි ඩන්ග්ලිසන්ගේ Practice of Medicine ග්රන්ථයේ පළමු සංස්කරණය තුළ ප්රකාශයට පත්කෙරිණි. වෝටර්ස් විසින් මෙය විස්තර කොට තිබුණේ "කෝරියා ප්රභේදයක් බවත්, කටවහරින් magrums නම් වූ බවත් ය." මෙහි කෝරියාව පිළිබඳ නිවැරදි විස්තරයකුත්, එහි වර්ධනය සහ රෝගයේ ප්රබල ආවේණිය පිළිබඳවත් සඳහන් විය.[95] 1846දී, චාල්ස් ගෝර්මන් ඇතැම් ප්රාදේශීය කලාප තුළ මෙම රෝගයේ ඉහළ ව්යාප්තියක් ඇති බව හඳුනාගත්තේ ය.[95] ෆිලඩෙල්ෆියාවේ ජෙෆර්සන් වෛද්ය විද්යාලයේ ඩන්ග්ලිසන්ගේ ශිෂ්යයන් වූ ගෝර්මන් සහ වෝටර්ස්ගෙන් ස්වායත්තව,[96] ජොහෑන් ක්රිස්ටියන් ලුන්ඩ් විසින් ද 1860දී මේ පිළිබඳ විස්තරයක් ගොඩනගා ඇත.[95] ඔහු විශේෂයෙන්ම පැවසූයේ නෝර්වේහි හුදකලා කඳුකර නිම්නයක් වූ සීට්ස්ඩැලන්හි පවුල් තුළ අචේතනික චලන සඳහා හේතුවෙන ආබාධයක් හා සම්බන්ධ ඩිමෙන්ෂියා තත්ත්වයක් සුලබව ව්යාප්ත වී ඇති බවයි.[97]
මෙම රෝගය පිළිබඳ පළමු සම්පූර්ණ විස්තර ඉදිරිපත් කරන ලද්දේ ජෝර්ජ් හන්ටිංටන් විසින් 1872දී ය. සමාන රෝග ලක්ෂණ පෙන්වන පවුලක පරම්පරා කිහිපයක සංයුක්ත වෛද්ය ඉතිහාසය අධ්යයනය කළ ඔහු, මේවායේ තත්ත්වය එකිනෙක හා සම්බන්ධ බව වටහාගත්තේ ය. ඔහු සිය පළමු පත්රිකාවේ රෝගය පිළිබඳ සවිස්තරාත්මක සහ නිවරුදි අර්ථ දැක්වීමක් ඉදිරිපත් කොට ඇත. විද්යාඥයින් විසින් මෙන්ඩලීය ප්රවේණිය යළි හඳුනා ගැනීමට වසර ගණනාවකට පෙර, හන්ටිංටන් විසින් මෙයට අලිංග වර්ණදේහ ප්රමුඛ ආවේණි රටාවක් ඇති බව විස්තර කොට ඇත.
"මෙහි ප්රවේණි ස්වභාවය පිළිබඳව. දෙමාපියන් දෙදෙනාම හෝ එක් අයකු රෝගය පෙන්වන විට ..., ප්රජනිතයෙන් එක් අයකු හෝ වැඩි සංඛ්යාවක් බොහෝවිට අවිවාදයෙන්ම රෝගයෙන් පෙළෙනු ඇත ... නමුත් යම් අවස්ථාවක මෙම දරුවන් රෝගයෙන් තොර වුවහොත්, මෙම පෙළ බිඳවැටෙන අතර මුල් ජනකයින්ගේ මුණුපුරන් සහ මීමුණුපුරන් මෙම රෝගයෙන් තොර වනු ඇත.".[93][98]
මෙම ආබාධය සහ කෝරියාව පිළිබඳ උනන්දුවක් දැක්වූ ශ්රීමත් විලිම් ඔස්ලර් හන්ටිංටන්ගේ පත්රිකාව දැක විමතියට පත්වූ අතර, ඔහු පැවසූයේ "වෛද්ය විද්යා ඉතිහාසයේ, රෝගයක් වඩාත් නිරවද්යව, ප්රස්තාරිකව සහ වඩාත් කෙටියෙන් විස්තර කළ හැකි අවස්ථා ඇත්තේ ස්වල්පයකි." යනුවෙනි.[95][99] හන්ටිංටන්ගේ රෝගය පිළිබඳ ඔස්ලර් දැක්වූ උනන්දුව සහ වෛද්ය විද්යා ක්ෂේත්රය වෙත වූ ඔහුගේ බලපෑම හේතුවෙන් වෛද්ය ප්රජාව අතර මෙම රෝගය පිළිබඳ දැනුම ශීඝ්රයෙන් ව්යාප්ත වීමට හේතු විය.[95] සියවසේ අගභාගය දක්වාම ලුවිස් තියෝෆිලේ ජෝසෆ් ලැන්ඩෞසි, ඩේසිරේ-මැග්ලොයර් බොර්නෙවිල්, කැමිලෝ ගොල්ගි, සහ ජෝසෆ් ජූල්ස් ඩෙජරින් වැනි යුරෝපීය විද්යාඥයෝ මෙම රෝගය කෙරෙහි උනන්දු වූහ. හන්ටිංටන්ගේ රෝගය පිළිබඳ සිදුකෙරුණු බොහෝ පර්යේෂණ යුරෝපීය සම්භවයක් ඇති ඒවායි.[95] 19වන සියවසේ අවසානය වන විට, හන්ටිංටන්ගේ රෝගය පිළිබඳ පර්යේෂණ සහ වාර්තා රැසක් රටවල් ගණනාවක ප්රකාශයට පත්කෙරිණි. මේ නිසා රෝගය ලෝක ව්යාප්ත තත්ත්වයක් ලෙස සැළකිණි.[95]
20වන සියවසේ දී මෙන්ඩලීය ප්රවේණිය යළි අනාවරණය කරගැනීමත් සමග, හන්ටිංටන්ගේ රෝගය අලිංග වර්ණදේහ ප්රමුඛ ආවේණියකට උදාහරණයක් ලෙස තාවකාලිකව භාවිතා විය.[95] ඉංග්රීසි ජාතික ජීව විද්යාඥ විලියම් බේට්සන් විසින් හන්ටිංටන්ගේ රෝගයට අලිංග වර්ණදේහ ප්රමුඛ ආවේණි රටාවක් ඇති බව සනාථ කිරීමට ආසාදිත පවුල්වල පෙළවැල් සටහන් භාවිතා කරන ලදී.[96] ප්රබල ආවේණි රටාව හේතුවෙන් ස්මිත් එලයි ජෙලිෆ් ඇතුළු පර්යේෂකයින් ගණනාවක් මේ පිළිබඳ අධ්යයනය කළ අතර, ඔවුන් පෙර අධ්යයන සමග පවුල් සාමාජිකයින් සම්බන්ධ කිරීමට උත්සාහ ගන්නා ලදී.[95] නිව් යෝක් ජනපදය පුරා තොරතුරු එක්රැස් කළ ජෙලිෆ් නව එංගලන්තයේ හන්ටිංටන්ගේ රෝගයේ වංශාවලිය පිළිබඳ ලිපි ගණනාවක් ප්රකාශයට පත්කළේ ය.[100] ජෙලිෆ්ගේ අධ්යයනය ඔහුගේ කොලීජියේ මිතුරා වූ චාල්ස් ඩේවන්පෝට්ගේ කුතුහලය ඇතිකිරීමට හේතු විය. ඩේවන්පෝට් විසින් එලිසබෙත් මන්සී හට එක්සත් ජනපදයේ නැගෙනහිර වෙරළ තීරයේ හන්ටිංටන්ගේ රෝගය සහිත පවුල් සහ ඔවුන්ගේ පෙළවැල් ගොඩනැගීමට යොමුකරන ලදී.[101] ඩේවන් මෙම තොරතුරු යොදා ගනිමින් රෝගයේ රෝග ලක්ෂණ මතුවන වයස් සීමාවේ විචලනය සහ ඇරඹීම පිළිබඳ ලේඛනගත කරන ලදී. ඔහු පැවසූයේ ඇමරිකා එක්සත් ජනපදයේ බොහෝ හන්ටිංටන් සිදුවීම් අතීතයේ රෝගීන් කිහිප දෙනකුගෙන් දායාද වූ ඒවා බවයි.[101] මෙම පර්යේෂණ තවත් පුළුල් කරමින් 1932දී පී. ආර්. වෙසී විසින් සමාජගත කරන ලද්දේ 1630දී එංගලන්තය අත්හැර බොස්ටන් වෙත පැමිණි සොහොයුරන් තිදෙනකු ඇමරිකාවේ හන්ටිංටන් රෝගයේ පූර්වජයන් බවයි.[102] මුල්කාලීන මුතුන් මිත්තන් විසින් රෝගය ස්ථාපිත කළ බවට වූ ප්රකාශය සහ මන්සී, ඩේවන්පෝට් හා වෙසීගේ කෘතිවල ඇතුළත් සුජනන නැඹුරුභාවය හේතුවෙන් හන්ටිංටන්ගේ රෝගය පිළිබඳ වැරදි වැටහීම් සහ අවිචාරවත් මතයක් බිහිවීමට හේතු විය.[96] මන්සී සහ ඩේවන්පෝට් විසින් ජනගත කළ තවත් මතයක් වූයේ අතීතයේ ඇතැම් හන්ටිංටන් රෝගීන් භූතාත්මවල ගොදුරු සහ මායාකර්මයන්ට ලක්වූවන් ලෙස සලකා සමාජයෙන් කොන් කිරීම සහ පිටුවහල් කිරීම සිදු වූ බවයි.[103][104] මෙම මතය සනාථ නොවූවකි. පර්යේෂකයින් විසින් මීට පටහැනි සාක්ෂි ද සොයාගෙන ඇත. උදාහරණයක් ලෙස ජෝජ් හන්ටිංටන් විසින් අධ්යයනය කළ පවුල විවෘතව හන්ටිංටන්ගේ රෝග ලක්ෂණ පෙන්වූ පුද්ගලයන්ට නවාතැන් ලබාදී තිබේ.[96][103]
මෙම තත්ත්වය හේතු සෙවීමේ පර්යේෂණ 1968දී වැඩිදියුණු වූ අතර කැලිෆෝනියාවේ ලොස් ඇන්ජලීස්හි විසූ මිල්ටන් වෙක්ස්ලර් විසින් ආවේණි රෝග පදනම (HDF) පිහිටුවන ලදී. ඔහු මනෝවිශ්ලේෂකයකු වූ අතර, ඔහුගේ බිරිඳ වන ලියොනෝර් සැබීන් එම වර්ෂයට පෙර වර්ෂයේ හන්ටිංටන්ගේ රෝගය සහිත තැනැත්තියක බව හඳුනාගැනීමට මීට හේතු විය.[105] වෙක්ස්ලර්ගේ භාර්යාවගේ සොහොයුරන් තිදෙනා ද මෙම රෝගයෙන් පෙළෙමින් සිටියහ. මෙම පදනම මගින් විද්යාඥයින් 100කට අධික සංඛ්යාවක් බඳවාගෙන හන්ටිංටන්ගේ රෝග සහයෝගීත්ව පර්යේෂණ ව්යාපෘතිය දියත් කරන ලදී. ඔවුහු වසර 10කට අධික කාලයක් වැය කරමින් මෙයට අදාළ ජානය හඳුනා ගැනීමට උත්සාහ දැරූහ.
HDF සංවිධානයට ස්තූතිවන්නට, 1979දී ආරම්භ වූ එ.ජ.-වෙනිසියුලා හන්ටිංටන්ගේ රෝග සහයෝගීත්ව පර්යේෂණ ව්යාපෘතිය 1983දී අදාළ ජානයේ නිශ්චිත පිහිටුම සොයාගැනීමට සමත් විය.[88] මෙය රෝගයේ අසාමාන්ය ලෙස ඉහළ ව්යාප්තියක් තිබූ බැරන්ක්විටාස් සහ ලැගුනේටාස් නැමැති හුදකලා වෙනිසියුලානු ගම්මාන ද්විත්වයේ ජනගහනය පිළිබඳ සිදුකළ පුළුල් පර්යේෂණයක ප්රතිඵලයකි.මෙයට පුද්ගලයින් 18,000කට අධික සංඛ්යාවක් දායක කරගැනිණි. මින් බොහෝදෙනකු තනි පවුලකින් පැවතෙන්නන් විය.
සෙසු නව නිමැවුම් වූ, මෙම ව්යාපෘතිය විසින් සංවර්ධනය කළ DNA-සලකුණු කිරීමේ ක්රමවේද මානව ගෙනෝම ව්යාපෘතිය දියත් කිරීමට මහෝපකාරී විය.[106] 1993දී, මෙම පර්යේෂණ කණ්ඩායම විසින් අදාළ ජානය 4p16.3 දී වෙන්කර ගන්නා ලදී.[107] මෙය ප්රවේණික ප්රතිබද්ධ විශ්ලේෂණය මගින් පථය සොයාගැනුණු පළමු අලිංග වර්ණදේහ රෝගය විය.[107][108]
එම කාලසීමාවේම, මෙම ආබාධයේ යන්ත්රණය හා සම්බන්ධ වැදගත් සොයාගැනීම් කිහිපයක්ම අනාවරණය විය. මේ අතරට ජානයේ දිග හා එහි බලපෑම සම්බන්ධ ඇනිටා හාර්ඩිංගේ පර්යේෂණ කණ්ඩායම වැදගත් වේ.[109]
1996දී වර්ධනය කෙරුණු පාරජානක මීයන් වැනි විවිධ සතුන් තුළ රෝගය ආදර්ශනයට හැකි වීම නිසා මහා පරිමාණයේ පර්යේෂණ කටයුතු දියුණු විය. මිනිසාට සාපේක්ෂව මෙම සත්ත්වයින් සතුව ශීඝ්ර පරිවෘත්තියක් සහ කෙටි ජීවිත කාලයක් තිබීම නිසා පර්යේෂණ ප්රතිඵල ඉක්මණින් ලැබිණි. 1997දී mHTT ඛණ්ඩ නැවීමේ දෝෂ සොයාගැනීම හේතුවෙන් ඉන් ඇතිවන න්යෂ්ටික අන්තර්ගතයන් අනාවරණය විය. මෙවැනි ප්රගමනයන් හේතුවෙන් රෝගයට සම්බන්ධ ප්රෝටීන, යෝග්ය ඖෂධ ප්රතිකාර, රැකබලාගැනීමේ ක්රම සහ ජානය පිළිබඳ වැඩිදුර පර්යේෂණ මෙහෙයවෙමින් පවතී.[95][110]
මෙම තත්ත්වය මුලින් හැඳින්වුණේ 'හන්ටිංටන්ගේ කෝරියාව' යන නාමයෙනි. සෑම රෝගියකුම තුළ කෝරියාව වර්ධනය නොවන බැවින් වර්තමානයේ ඒ සඳහා 'හන්ටිංටන්ගේ රෝගය' යන වදන භාවිතා වේ.[111]
සමාජය සහ සංස්කෘතිය
[සංස්කරණය]ආචාර ධර්ම
[සංස්කරණය]හන්ටිංටන්ගේ රෝගය විශේෂයෙන්ම, රෝගය සඳහා වන අයැදුම් පරීක්ෂණය හා සම්බන්ධ ආචාර ධර්ම වාද විෂයයන්ට ලක්වී ඇත. මෙම ප්රවේණි පරීක්ෂා සඳහා වන විෂයයන් අතරට යම් තැනැත්තකු ප්රවේණි පරීක්ෂාවට යෝග්යදැයි දැනගැනීමට කෙතරම් පරිණත විය යුතු ද, ප්රතිඵලවල රහස්යභාවය සහ විශ්වසනීයත්වය තහවුරු කිරීම, සමාගම්වලට මෙම ප්රතිඵල රැකියා, ජීවිත රක්ෂණ සහ මූල්යමය ගැටලු සම්බන්ධ තීරණ ගැනීමට භාවිතයට අවසර දිය යුතු ද යන්න අදාළ වේ. 1910දී චාල්ස් ඩේවන්පෝට් විසින් සුජනක ව්යාපාරය හා සමගාමීව හන්ටිංටන්ගේ රෝගය ඇතුළු ඇතැම් රෝග සහිත පෙදෙස්වල සිට පැමිණෙන ජනයා අනිවාර්ය වන්ධ්යකරණයකට හෝ සංක්රමණ පාලනයකට ලක්කළ යුතු බවට මතයක් ඉදිරිපත් කරන ලදී.[112] නාලස්ථ සංසේචනය (In vitro fertilization) අනුගමනයේ දී එයට කලල භාවිතය පිළිබඳව ද සැලකිය යුතු වාදවිෂයයන් රැසක් පවතියි. ඇතැම් හන්ටිංටන්ගේ රෝග පර්යේෂණ පිළිබඳ ආචාර විද්යානුකූල මතභේදයන් පැනනැගී ඇත්තේ එයට සත්ත්ව පරීක්ෂා සහ කලල පියවි සෛල භාවිතා වන බැවිනි.[113][114]
හන්ටිංටන්ගේ රෝගය සඳහා නිශ්චිත රෝග විනිශ්චය පරීක්ෂාව ගොඩනැගීමේ දී පුද්ගලයාගේ ප්රතිඵල භාවිතය හා සම්බන්ධ සමාජයීය, නීතිමය, සහ ආචාරධර්මානුකූල කරුණු රැසක් සලකා බැලිය යුතු ය.[115][116] බොහෝ මෙහෙයුම් ප්රතිපත්ති සහ පරීක්ෂා ක්රමවේද කෙරෙහි එහි ප්රතිඵල අනාවරණය සහ රහස්යභාවය රැකගැනීම පිළිබඳ දැඩි ක්රියාමාර්ග පවතියි. එමගින් පුද්ගලයින්ට එම ප්රතිඵල ලබාගන්නා දිනය, සහ ආකාරය මෙන්ම එම ප්රතිඵල ලබාදිය හැකි පුද්ගලයින් පිළිබඳසීමා පැනවේ.[23] ජීවිත රක්ෂණ හෝ රැකියා වැනි කටයුතුවල පුද්ගලයකු ඇගයුමේ දී මූල්යමය සංස්ථාපිතයන් සහ ව්යාපාර ප්රවේණි පරීක්ෂා ප්රතිඵල භාවිත කළ යුතු ද යන ප්රශ්නයට මුහුණපා සිටියි. එක්සත් රාජධානියේ රක්ෂණ සමාගම් 2017 වර්ෂය තෙක් £500,000 යටතේ රක්ෂණ ප්රතිපත්ති රචනා කිරීමේ දී ප්රවේණි තොරතුරු භාවිතා නොකිරීමට එකඟ වී ඇත. නමුත් පැහැදිළිවම හන්ටිංටන්ගේ රෝගය මෙම ගිවිසුමට ඇතුළත් කොට නැත.[117][118] පසුකාලීනව රෝගය ඇරඹෙන ප්රතිකාර නොමැති සෙසු ප්රවේණි ආබාධ සඳහා දරුවකුට හෝ වැඩිහිටියකුට පූර්ව-රෝගලක්ෂණික පරීක්ෂාවක් සිදුකළ යුතු ද යන්න ආචාරවිද්යානුකූලව ප්රශ්නාර්ථයකි. එයට හේතුව එම පුද්ගලයන්ට කිසිදු වෛද්යය වාසියක් නොවීමයි. ඥානාත්මක වශයෙන් වැඩුණු යැයි සැලකිය හැකි පුද්ගලයන්ට පමණක් මෙම පරීක්ෂාව සිදුකළ යුතු බවට පිළිගැනීමක් ඇත. නමුත් දරුවකුට මෙම පරීක්ෂාවක් සිදු කිරීමට දෙමාපියන්ට අයිතියක් ඇති බවට මීට විරුද්ධ එකඟතාවක් ද ඇත. ක්රියාකාරී ප්රතිකාර මඳ හෙයින්, වයස් සීමාවක් අනුව යෝග්ය යැයි නොසැලකෙන පුද්ගලයකු පරීක්ෂාවට ලක්කිරීම බොහෝ අවස්ථාවල ආචාර් ධර්ම විරෝධී යැයි පිළිගැනේ.[38][119][120]
දරුවා රෝගය සහිතව උපත නොලබන බව සනාථ කරගැනීමට පුරඃප්රසව ප්රවේණි පරීක්ෂා හෝ පූර්වඅධිරෝපණ ප්රවේණි රෝග විනිශ්චය සම්බන්ධයෙන් ද පිළිපැදිය යුතු ආචාර ධර්ම පවතී.[121] උදාහරණයක් ලෙස, පුරඃප්රසව පරීක්ෂා නිසා සිදුකළ හැකි ගබ්සා කිරීම් ඇතැමකු විසින් අනුමත නොකරන්නට පුළුවන.[121] මෙය ප්රමුඛ රෝගයක් නිසා, ඇතැම් දෙමාපියන්ට සිය රෝග විනිශ්චය ප්රතිඵල දැනගැනීමට අවැසි නොවන අවස්ථා ද එළැඹිය හැක. මේ නිසා මෙම ක්රියාවලියේ දී එය දෙමාපියන්ගෙන් රහසක්ව තබා ගැනීමට සිදුවේ.[121]
සහාය සංවිධාන
[සංස්කරණය]
1968දී, හන්ටිංටන්ගේ රෝගය පිළිබඳ සිය බිරිඳගේ පවුල තුළින් අත්දැකීම් ලත් වෛද්ය මිල්ටන් වෙක්ස්ලර් විසින් ආවේණි රෝග පදනම (HDF) ආරම්භ කරන ලදී. මෙහි අරමුණ වන්නේ පර්යේෂණ සමායෝජනය සහ සහාය වීම මගින් ප්රවේණි රෝග සුවපත් කිරීමයි.[8] මෙම පදනම සහ වෙක්ස්ලර්ගේ දියණිය වූ නැන්සි වෙක්ස්ලර් හන්ටිංටන් රෝගයේ ජානය සොයාගැනීමට දායක වූ වෙනිසියුලාවේ පර්යේෂක කණ්ඩායමේ වැදගත් සාමාජිකයන් විය.[8]
දළ වශයෙන් HDF ගොඩනැගූ සමයේම, මාජරී ගුත්රී විසින් හන්ටිංටන්ගේ රෝගය සමග සටන් කිරීමේ කමිටුව (වර්තමාන ඇමරිකාවේ හන්ටිංටන්ගේ රෝග සමාජය) පිහිටුවන ලද්දේ, ඇගේ සැමියා වූ වූඩි ගුත්රී හන්ටිංටන් රෝගය හේතුවෙන් මියයාමෙන් පසුවයි.[9]
එතැන් සිට, හන්ටිංටන්ගේ රෝගය පිළිබඳ මහජන දැනුවත්භාවය වැඩි කිරීමේ අරමුණින් ලෝකය වටා බොහෝ රටවල සහාය සහ පර්යේෂණ සංවිධාන බිහි විය. මේවායින් කිහිපයක් සම්බන්ධීකරණ සංවිධාන ලෙස ක්රියා කරයි. උදාහරණයක් වශයෙන් අන්තර්ජාතික හන්ටිංටන් සංවිධානය සහ යුරෝපීය HD ජාලය දැක්විය හැක.[122] බොහෝ සහාය සංවිධාන මගින් වාර්ෂික හන්ටිංටන් රෝග දැනුවත් කිරීමේ වැඩසටහන් සංවිධානය කරනු ලබයි. ඇතැම් වැඩසටහන් අදාළ රජයයන්ගේ සහාය ඇතිව සිදුවේ. උදාහරණයක් ලෙස, එක්සත් ජනපද සෙනට් සභාව විසින් ජූනි 6 "ජාතික හන්ටිංටන්ගේ රෝග දැනුම්වත් දිනය" ලෙස නම්කොට ඇත.[123]
මූල්යමය ආධාර සපයමින් හන්ටිංටන් රෝගය පිළිබඳ ලොව පුරා පර්යේෂණ මෙහෙයවීමට සහාය දක්වන විශාලතම අනුග්රාහකයා[124] CHDI පදනමයි. ලාභ-නොලබන එක්සත් ජනපද ජෛවවෛද්ය විද්යා පදනමක් වන මෙහි අරමුණ වන්නේ "හන්ටිංටන්ගේ රෝගය ප්රමාද කරන හෝ ක්රියාකාරී වීම මන්දනය කරන ඖෂධ ශීඝ්රයෙන් අනාවරණය කර ගැනීමයි".[125] CHDI මුලින් හැඳින්වුණේ උසස් Q පදනම යනුවෙනි. 2006දී එම ආයතනය විසින් හන්ටිංටන්ගේ රෝග පර්යේෂණ සඳහා ඇ.ඩො. මිලියන 50ක් වියදම් කොට තිබේ.[124] CHDI ආයතනය බොහෝ ගෝලීය ආයතනික සහ වාණිජමය විද්යාගාර සමග සහයෝගයෙන් කියා කරන අතර, පර්යේෂණ ව්යාපෘති කළමනාකරණයට සහ ආධාර සැපයීමට එය උපකාරී වේ.[126] හන්ටිංටන්ගේ රෝගය වැළඳුණු පුද්ගලයින් දැනුම්වත් කිරීමට සහ ආධාර වීමට බොහෝ සංවිධාන පවතී.
පර්යේෂණ දිශානති
[සංස්කරණය]හන්ටිංටන්ගේ රෝගයේ යන්ත්රණය පිළිබඳ පර්යේෂණ මගින් HTTහි කෘත්යය, ඉන් mHTT වෙනස්වන හෝ අන්තර්ක්රියා කරන ප්රමාණය, සහ රෝගය නිසා ඇතිවන මොළයේ ව්යාධිවේදය හැදෑරීම අරමුණු කෙරේ. පර්යේෂණ සිදුකරන්නේ නාලස්ථ (in vitro) ක්රමවේද, සත්ත්ව ආදර්ශක සහ ස්වච්ඡා මිනිසුන් උපකාරයෙනි. සත්ත්ව ආදර්ශක රෝගයේ මූලික යන්ත්රණ හැදෑරීමේ දී අර්බුදකාරී වන අතර. ඒවා උපකාරී වන්නේ ඖෂධ සංවර්ධනයේ මුල්කාලීන අවධි සඳහා පමණි.[110] රසායනික ප්රේරිත මොළයේ ආබාධ සහිත සත්ත්වයින් HD-වැනි රෝග ලක්ෂණ පෙන්වූ අතර, ඔවුන් මුලින් යොදාගැනිණි. නමුත් ඒවා රෝගයේ සත්ය ස්වරූපය පෙන්වූයේ නැත.[127] හේතුකාරක ජානයේ හඳුනාගැනීමත් සමග බොහෝ පාරජානක සත්ත්ව ආකෘති ආධාර කරගත හැකි විය. මේ අතරට නෙමටෝඩා පණුවන්, Drosophila පළතුරු මැස්සන්, මියන්, බැටලුවන් සහ වඳුරන් ඇතුළත් විය. මොවුන් තුළ විකෘති හන්ටිංටින් ජානය ඇතුළත් වූ හෙයින් ප්රගාමී ස්නායුපරිහානිය සහ හන්ටිංටින් වැනි සහලක්ෂණ වර්ධනය විය.[110]
හන්ටිංටන්ගේ රෝගය යැළැක්වීමට හෝ එහි වර්ධනය ප්රමාද කරවීමට නොයෙකුත් පර්යේෂණ ක්රියාත්මක වෙමින් පවතී. රෝගය-අඩු කිරීමේ උපක්රම ප්රධාන ආකාර තුනකට වර්ග කළ හැක: එනම් විකෘති හන්ටිංටින් ප්රෝටීන මට්ටම අඩු කිරීම (ජාන නිහඬ කරවීම ඇතුළු); නියුරෝනවල පැවැත්ම වැඩිදියුණු කිරීම සඳහා ප්රෝටීනය මගින් විශේෂිත සෛලිය පථ සහ යන්ත්රණවලට සිදුකළ හානිය අවම කිරීම (ප්රෝටීන සමස්ථිතිය සහ හිස්ටෝන් ඩිඇසිටයිලේස් නිෂේධනය ඇතුළු); සහ හානිවූ නියුරෝන ප්රතිස්ථාපනයට ක්රියාමාර්ග ගැනීමයි. මීට අමතරව, මොළයේ කෘත්යය වැඩිදියුණු කිරීම අරමුණු කරගත් නව්ය චිකිත්සක ක්රම තවමත් අත්හදා බැලෙමින් පවතී. මේවා මගින් රෝගය අඩු කිරීමේ චිකිත්සක කමවලට වඩා චිරකාලීන ප්රතිකාර ක්රම වර්ධනය කිරීම අරමුණු කෙරේ. මේ අතරට ෆොස්ෆොඩයිඑස්ටරේස් නිෂේධක ආදිය ඇතුළත් ය.[128]
හන්ටිංටින් නිපදවීම අඩු කිරීම
[සංස්කරණය]ජාන නිහඬ කිරීම මගින් විකෘති ප්රෝටීනය නිපදවීම අඩු කිරීම අරමුණු කෙරේ. එයට හේතුව හන්ටිංටින් විෂැති ප්රෝටීනයක් සඳහා කේතය සපයන තනි ප්රමුඛ ජානයකින් යුතු වීමයි. මීයන් යොදා ගනිමින් සිදුකළ ජාන නිහඬ කිරීමේ පර්යේෂණ මගින් පෙනීගොස් ඇත්තේ mHTT හි ප්රකාශනය අඩු වන විට, රෝග ලක්ෂණ වඩාත් යහපත් තත්ත්වයට හැරෙන බවයි.[129] ඇලීල-නොවන විශේෂිත RNAi සහ ASO ජාන නිහඬ කිරීමේ ආරක්ෂිතභාවය මීයන් සහ මිනිසවැනි ප්රයිමේටාවන්ගේ මොළ තුළින් වටහාගත හැක.[130][131] ඇලීල-විශේෂිත නිහඬ කිරීමේ ක්රමවේදවල දී, විකෘති HTT ජානය නිහඬ කරවන අතර, HTT වල්-දර්ශයේ කිසිදු වෙනසක් නොකෙරේ. මෙය සිදුකිරීමේ එක් ක්රමයක් මගින් තනි ඇලීලයක අන්තර්ගත බහුරූපීතාවන් හඳුනාගැනීම සහ තනි එක් විකෘති ඇලීලයක පමණක් ඇති බහුරූපීතාවන් ඉලක්ක කරගත් නිහඬකාරක ඖෂධ නිර්මාණය කෙරේ.[132] මිනිස් හන්ටිංටන් රෝගීන් දායක කරගත් පළමු 'ජාන නිහඬකරණ' අත්හදා බැලීම 2015 වර්ෂයේ ඇරඹිණි. අයෝනිස් ඖෂධකරුවන් විසින් නිපදවන ලද IONIS-HTTRx හි සුර්ක්ෂිතතාව පරීක්ෂා කෙරුණු මෙය මෙහෙයවන ලද්දේ ස්නායුවේදය පිළිබඳ UCL ආයතනය විසිනි.[133][134] 2015දී නව 'තනි-අණු ගණන' ප්රතිශක්ති පරීක්ෂා මගින් හන්ටිංටන් රෝග විකෘති වාහකයන් තුළින් පළමුවරට මස්තිෂ්කසුෂුම්නා තරලයේ තිබී විකෘති හන්ටිංටින් අනාවරණය කරගන්නා ලදී.[135] මෙලෙසින් හන්ටිංටින්-පහත හෙළීමේ ප්රතිකාර ක්රම නිසි පරිදි ක්රියාකරන්නේ දැයි සොයාබැලීමට ඍජු මාර්ගයක් ලැබේ.[136][137]
සෛලවල පැවැත්ම වැඩිදියුණු කිරීම
[සංස්කරණය]විකෘති හන්ටිංටින් පවතින විට භාවිතා වන සෛල පැවැත්ම වැඩිදියුණු කිරීමේ ක්රමවලදී හිස්ටෝන් ඩිඇසිටයිලේස් නිෂේධකය භාවිතා කොට ප්රතිලේඛන යාමනය නිවැරදි කිරීම, හන්ටිංටින් සමාහරණය උස් පහත් කිරීම, පරිවෘත්තිය හා මයිටොකොන්ඩ්රීය කෘත්යය වැඩිදියුණු කිරීම සහ උපාගමවල කෘත්යය ප්රතිෂ්ඨාපනය සිදුකෙරේ.[129]
නියුරෝනීය ප්රතිස්ථාපනය
[සංස්කරණය]පියවි සෛල චිකිත්සාව යනු මොළයේ ආසාදිත ප්රදේශවල හානි වූ නියුරෝන ප්රතිස්ථාපනය කරමින් පියවි සෛල බද්ධ කිරීමයි. මෙම තාක්ෂණය සත්ත්ව ආදර්ශක සහ මූලික මිනිස් සායනික අත්හදා බැලීමේ පරීක්ෂණ මගින් මිශ්ර ප්රතිඵල ලබා දී ඇත.[138] මේවායේ අනාගත චිකිත්සීය විභවය කුමක් වුව ද, විද්යාගාරවල හන්ටිංටන්ගේ රෝගය හැදෑරීමේ දී පියවි සෛල වටිනා අංගයකි.[139]
සායනික අත්හදා බැලීම්
[සංස්කරණය]හන්ටිංටව්ගේ රෝගය පිළිබඳ නව පර්යේෂණ ප්රතිකාර සඳහා සායනික අත්හදා බැලීම් ගණනාවක් සිදුවෙමින් පවතී.[140]
රෙමැසිමයිඩ්, සහඑන්සයිම Q10, රිලුසෝල්, ක්රියටින්, මිනොසයික්ලින්, එතිල්-EPA, ෆීනයිල්බියුටයිරේට් සහ ඩයිමෙබොන් වැනි සංකීර්ණ මිනිසුන් යොදාකළ අත්හදාබැලීම්වල දී හන්ටිංටන්ගේ රෝගය ප්රමාද කිරීමට හෝ වැළැක්වීමට අපොහොසත් වී තිබේ.[141]
ආශ්රේයයන්
[සංස්කරණය]- ^ a b c d e f "Huntington's Disease Information Page: National Institute of Neurological Disorders and Stroke (NINDS)". NINDS. ජනවාරි 28, 2016. සම්ප්රවේශය 19 ජූලි 2016.
- ^ a b c d e f g h i දයාලු, පී.; ඇල්බින්, ආර්. එල්. (පෙබරවාරි 2015). "Huntington disease: pathogenesis and treatment". Neurologic Clinics. 33 (1): 101–14. doi:10.1016/j.ncl.2014.09.003. PMID 25432725.
- ^ a b c d වෝර්බි, එස්. සී.; ග්රැහැම්, ආර්. කේ.; හේඩ්න්, එම්. ආර්.; පේගන්, ආර්. ඒ.; ඇඩම්, එම්. පී.; ආර්ඩිංගර්, එච්. එච්.; වැලේස්, එස්. ඊ.; අමේමියා, ඒ.; බීන්, එල්. ජේ. එච්.; බර්ඩ්, ටී. ඩී.; ෆොං, සී. ටී.; මෙෆෝර්ඩ්, එච්. සී.; ස්මිත්, ආර්. ජේ. එච්.; ස්ටීවන්ස්, කේ. (2014). "Huntington Disease". PMID 20301482.
{{cite journal}}: Cite journal requires|journal=(help) - ^ a b c d e f g ෆ්රෑන්ක්, එස්. (ජනවාරි 2014). "Treatment of Huntington's disease". Neurotherapeutics : the journal of the American Society for Experimental NeuroTherapeutics. 11 (1): 153–60. doi:10.1007/s13311-013-0244-z. PMC 3899480. PMID 24366610.
- ^ ඩූර්, ඒ.; ගාර්ගියුලෝ, එම්.; ෆේන්ගෝල්ඩ්, ජේ. (නොවැම්බර් 2012). "The presymptomatic phase of Huntington disease". Revue neurologique. 168 (11): 806–8. doi:10.1016/j.neurol.2012.07.003. PMID 22902173.
- ^ වේල්, ටී. සී.; කාර්ඩෝසෝ, එෆ්. (2015). "Chorea: A Journey through History". Tremor and other hyperkinetic movements (නිව් යෝක්, N.Y.). 5. doi:10.7916/D8WM1C98. PMC 4454991. PMID 26056609.
- ^ a b "Learning About Huntington's Disease". www.genome.gov. සම්ප්රවේශය 19 ජූලි 2016.
- ^ a b c d "History of the HDF". Hereditary Disease Foundation. සම්ප්රවේශය 18 නොවැම්බර් 2015.
- ^ a b "Huntington's Disease Society of America – Our History". Huntington's Disease Society of America. 2008. සම්ප්රවේශය 17 මාර්තු 2009.
- ^ a b c d වැන් ඩුයිජින්, ඊ; කිංමා ඊ එම්; වැන් ඩර් මාස්ට් ආර්. සී. (2007). "Psychopathology in verified Huntington's disease gene carriers". J Neuropsychiatry Clin Neurosci. 19 (4): 441–8. doi:10.1176/appi.neuropsych.19.4.441. PMID 18070848.
{{cite journal}}: Vancouver style error: name in name 1 (help) - ^ a b c d e f g h i j k l වෝකර් එෆ්. ඕ. (2007). "Huntington's disease". Lancet. 369 (9557): 218–28. doi:10.1016/S0140-6736(07)60111-1. PMID 17240289.
- ^ a b c "Huntington Disease". genereviews bookshelf. වොෂිංටන් විශ්වවිද්යාලය. 19 ජූලි 2007. සම්ප්රවේශය 12 මාර්තු 2009.
- ^ හැමන්ඩ් කේ., ටාටුම් බී. (26 ජූනි 2010). "The Behavioral Symptoms of Huntington's Disease". Huntington's Outreach Project for Education, at Stanford. සම්ප්රවේශය 4 අගෝස්තු 2014.
{{cite web}}: Cite has empty unknown parameter:|1=(help); Vancouver style error: punctuation in name 1 (help) - ^ a b ක්රෙමර් බී. (2002). "Clinical neurology of Huntington's disease". In බේට්ස් ජී., හාපර් පී., ජෝන්ස් එල්. (eds.). Huntington's Disease – තෙවන සංස්කරණය. ඔක්ස්ෆර්ඩ්: ඔක්ස්ෆර්ඩ් විශ්වවිද්යාලීය මුද්රණාලය. pp. 28–53. ISBN 0-19-851060-8.
{{cite book}}: Vancouver style error: punctuation in name 1 (help) - ^ වේගල් ඒ. සී., වේගල් එස්. ඒ., මාර්කෝවා අයි. එස්., බෙරියොස් ජී. ඊ. (2000). "Psychiatric Morbidity in Huntington's disease". Neurology, Psychiatry and Brain Research (8): 5–16.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b c d e f g h වෝකර් එෆ්. ඕ. (2007). "Huntington's disease". Lancet. 369 (9557): 218–28 [219]. doi:10.1016/S0140-6736(07)60111-1. PMID 17240289.
- ^ a b c d e f g h මොන්ටෝයා ඒ., ප්රයිස් බී. එච්., මෙනියර් එම්., ලිපේජ් එම්. (2006). "Brain imaging and cognitive dysfunctions in Huntington's disease" (PDF). J Psychiatry Neurosci. 31 (1): 21–9. PMC 1325063. PMID 16496032. 2016-03-23 දින මුල් පිටපත (PDF) වෙතින් සංරක්ෂණය කරන ලදී. සම්ප්රවේශය 1 අප්රේල් 2009.
{{cite journal}}: More than one of|archivedate=and|archive-date=specified (help); More than one of|archiveurl=and|archive-url=specified (help); Vancouver style error: punctuation in name 1 (help) - ^ අසිස් එන් ඒ; වැන් ඩර් මාර්ක් එම් ඒ; පිජ්ල් එච්; ඕල්ඩි රිකර්ට් එම් ජී; බ්ලෝයම් බී ආර්; රූස් ආර්. ඒ. (2008). "Weight loss in neurodegenerative disorders". J. Neurol. 255 (12): 1872–80. doi:10.1007/s00415-009-0062-8. PMID 19165531.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ "Booklet by the Huntington Society of Canada" (PDF). Caregiver's Handbook for Advanced-Stage Huntington Disease. HD Society of Canada. 11 අප්රේල් 2007. සම්ප්රවේශය 10 අගෝස්තු 2008.
- ^ ගැග්නොන් ජේ එෆ්; පෙටිට් ඩී; ලැට්රේල් වී; මොන්ට්ප්ලේසිර් ජේ. (2008). "Neurobiology of sleep disturbances in neurodegenerative disorders". Curr. Pharm. Des. 14 (32): 3430–45. doi:10.2174/138161208786549353. PMID 19075719.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ මරේ ඊ ඩී; බට්නර් එන්; ප්රයිස් බී. එච්. (2012). "Depression and Psychosis in Neurological Practice". In බ්රැඩ්ලි ඩබ් ජී; ඩැරොෆ් ආර් බී; ෆෙනිචෙල් ජී එම්; ජැන්කොවික් ජේ. (ed.). Bradley's neurology in clinical practice (6වන ed.). ෆිලඩෙල්ෆියා, PA: එල්සිවියර්/සෝන්ඩර්ස්. p. 108. ISBN 1-4377-0434-4.
{{cite book}}: Vancouver style error: punctuation in name 1 (help) - ^ වැන් ඩර් බර්ග් ජේ එම්; බ්ජෝක්විස්ට් එම්; බ්රන්ඩින් පී. (2009). "Beyond the brain: widespread pathology in Huntington's disease". Lancet Neurol. 8 (8): 765–74. doi:10.1016/S1474-4422(09)70178-4. PMID 19608102.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b c d e f g h i j k l m n o p q r s t වෝකර් එෆ්. ඕ (2007). "Huntington's disease". Lancet. 369 (9557): 218–28 [221]. doi:10.1016/S0140-6736(07)60111-1. PMID 17240289.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x වෝකර් එෆ්. ඕ. (2007). "Huntington's disease". Lancet. 369 (9557): 218–28 [220]. doi:10.1016/S0140-6736(07)60111-1. PMID 17240289.
- ^ කැස්ටුනෝ එම්; බැනෝ එච්; සුසුකි කේ. (2008). "Molecular genetics and biomarkers of polyglutamine diseases". Curr. Mol. Med. 8 (3): 221–34. doi:10.2174/156652408784221298. PMID 18473821.
{{cite journal}}: Invalid|display-authors=ඇතුළු පිරිස(help); Vancouver style error: punctuation in name 1 (help) - ^ a b වෝකර් එෆ්. ඕ. (2007). "Huntington's disease". Lancet. 369 (9557): 218–28 [222]. doi:10.1016/S0140-6736(07)60111-1. PMID 17240289.
- ^ නැන්ස් එම් ඒ; මයර්ස් ආර්. එච්. (2001). "Juvenile onset Huntington's disease—clinical and research perspectives". Ment Retard Dev Disabil Res Rev. 7 (3): 153–7. doi:10.1002/mrdd.1022. PMID 11553930.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ පැසාර්ජ් ඊ. (2001). Color Atlas of Genetics (2වන ed.). තියේම්. p. 142. ISBN 0-86577-958-9.
- ^ රිඩ්ලි ආර් එම්; ෆ්රිත් සී ඩී; ක්රෝ ටී ජේ; කොනේලි පී. එම්. (1988). "Anticipation in Huntington's disease is inherited through the male line but may originate in the female". Journal of Medical Genetics. 25 (9): 589–595. doi:10.1136/jmg.25.9.589. PMC 1051535. PMID 2972838.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ සෙමාකා ඒ; ක්රයිටන් එස්; වෝර්බි එස්; හේඩ්න් එම්. ආර්. (2006). "Predictive testing for Huntington disease: interpretation and significance of intermediate alleles". Clin. Genet. 70 (4): 283–94. doi:10.1111/j.1399-0004.2006.00668.x. PMID 16965319.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help); no-break space character in|vauthors=at position 7 (help) - ^ වෙක්ස්ලර් එන් එස්; යන්ග් ඒ බී; ටැන්සි ආර් ඊ; ට්රැවර්ස් එච්; ස්ටාරොස්ටා-රුබින්ස්ටයින් එස්; පෙනී ජේ බී; ස්නොඩ්ග්රාස් එස් ආර්; ෂූල්සන් අයි; ගෝමස් එෆ්; රේමස් ඇරෝයෝ එම්. ඒ. (1987). "Homozygotes for Huntington's disease". Nature. 326 (6109): 194–197. doi:10.1038/326194a0. PMID 2881213.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ස්ක්විටියේරි එෆ්; ගැලෙරා සී; කැනෙලා එම්. (2003). "Homozygosity for CAG mutation in Huntington disease is associated with a more severe clinical course". Brain. 126 (Pt 4): 946–55. doi:10.1093/brain/awg077. PMID 12615650.
{{cite journal}}: Invalid|display-authors=ඇතුළු පිරිස(help); Vancouver style error: punctuation in name 1 (help) - ^ ගොහ්ලර් එච්; ලැලොව්ස්කි එම්; ස්ටෙල්සල් යූ. (2004). "A protein interaction network links GIT1, an enhancer of Huntingtin aggregation, to Huntington's disease". Mol. Cell. 15 (6): 853–65. doi:10.1016/j.molcel.2004.09.016. PMID 15383276.
{{cite journal}}: Invalid|display-authors=ඇතුළු පිරිස(help); Vancouver style error: punctuation in name 1 (help) - ^ ග්ලැජ්ච්, කේ. ඊ.; සැඩ්රි-වැකිලි, ජී. (2015). "Epigenetic Mechanisms Involved in Huntington's Disease Pathogenesis". Journal of Huntington's disease. 4 (1): 1–15. PMID 25813218.
- ^ හාර්ජස් පී; වැන්කර් ඊ. ඊ. (2003). "The hunt for huntingtin function: interaction partners tell many different stories". Trends Biochem. Sci. 28 (8): 425–33. doi:10.1016/S0968-0004(03)00168-3. PMID 12932731. සම්ප්රවේශය 27 අප්රේල් 2009.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b c කැටනියෝ ඊ; සුකැටෝ සී; ටාර්ටරි එම්. (2005). "Normal huntingtin function: an alternative approach to Huntington's disease". Nat. Rev. Neurosci. 6 (12): 919–30. doi:10.1038/nrn1806. PMID 16288298.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b c d e රුබින්ස්ටයින් ඩී සී; කාර්මිචෙල් ජේ. (2003). "Huntington's disease: Molecular basis of neurodegeneration". Expert Rev Mol Med. 5 (20): 1–21. doi:10.1017/S1462399403006549. PMID 14585171.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b බ්ලොච් එම්; හේඩ්න් එම්. ආර්. (1990). "Opinion: predictive testing for Huntington disease in childhood: challenges and implications". Am. J. Hum. Genet. 46 (1): 1–4. PMC 1683548. PMID 2136787.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b c d බේට්ස්, ගිලියන් පී.; ඩෝර්සි, රේ; ගුසෙලා, ජේම්ස් එෆ්.; හේඩ්න්, මයිකල් ආර්.; කායි, ක්රිස්; ලීවිට්, බ්ලෙයාර් ආර්.; නැන්ස්, මාර්තා; රොස්, ක්රිස්ටෝෆර් ඒ.; ස්කැහිල්, රේචල් අයි.; වේටසෙල්, රොනල්ඩ්; වයිල්ඩ්, එඩ්වඩ් ජේ.; ටැබ්රිසි, සාරා ජේ. (23 අප්රේල් 2015). "Huntington disease". Nature Reviews Disease Primers: 15005. doi:10.1038/nrdp.2015.5.
- ^ සැඩ්රි-වැකිලි ජී; චා ජේ. එච්. (2006). "Mechanisms of Disease: histone modifications in Huntington's disease". Nature Clinical Practice Neurology. 2 (6): 330–338. doi:10.1038/ncpneuro0199. PMID 16932577.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ පර්විස් ඩී, ඔගස්ටීන් ජී. ඒ., ෆිට්ස්පැට්රික් ඩී., හෝල් ඩබ්., ලැමන්ටියා ඒ. එස්., මැක්නමාරා ජේ. ඕ., විලියම්ස් එස්. එම්. (2001). "Modulation of Movement by the Basal Ganglia – Circuits within the Basal Ganglia System". In පර්විස් ඩී. (ed.). Neuroscience (2වන ed.). Sunderland, MA: Sinauer Associates. ISBN 0-87893-742-0. සම්ප්රවේශය 1 අප්රේල් 2009.
{{cite book}}: Unknown parameter|chapterurl=ignored (help); Vancouver style error: name in name 1 (help) - ^ ලොබ්සිගර් සී එස්; ක්ලෙව්ලන්ඩ් ඩී. ඩබ්. (2007). "Glial cells as intrinsic components of non-cell autonomous neurodegenerative disease". Nat. Neurosci. 10 (11): 1355–60. doi:10.1038/nn1988. PMC 3110080. PMID 17965655.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b ක්රොස්මන් ඒ. ආර්. (2000). "Functional anatomy of movement disorders" (PDF). J. Anat. 196 (4): 519–25. doi:10.1046/j.1469-7580.2000.19640519.x. PMC 1468094. PMID 10923984.[permanent dead link]
- ^ ඩෆී, ජෝසෆ් (2013). Motor Speech Disorders: Substrates, Differential Diagnosis, and Management, 3වන සංස්. ශාන්ත ලුවිස්, මිසූරි: එල්සිවියර්. pp. 196–7.
{{cite book}}: no-break space character in|location=at position 14 (help) - ^ a b උපුටාදැක්වීම් දෝෂය: අනීතික
<ref>ටැගය;urlNature Clinical Practice Neurology | Mechanisms of Disease: histone modifications in Huntingtons disease | Articleනමැති ආශ්රේයන් සඳහා කිසිදු පෙළක් සපයා නොතිබුණි - ^ a b "Analysis of Strand Slippage in DNA Polymerase Expansions of CAG/CTG Triplet Repeats Associated with Neurodegenerative Disease – JBC".
- ^ ස්ටෙෆාන් ජේ; බොඩායි එල්; පැලොස් ජේ. (18 ඔක්තෝබර් 2001). "Histone deacetylase inhibitors arrest polyglutamine-dependent neurodegeneration in Drosophila". Nature. 413: 739–743. doi:10.1038/35099568.
{{cite journal}}: Invalid|display-authors=ඇතුළු පිරිස(help); Vancouver style error: punctuation in name 1 (help) - ^ ගේලාර්ඩ් එෆ්. (1 මැයි 2007). "Huntington's disease". Radiology picture of the day. www.radpod.org. සම්ප්රවේශය 24 ජූලි 2009.
- ^ රාඕ ඒ කේ; මියුරටරි එල්; ලුවිස් ඊ ඩී; මොස්කොවිට්ස් සී බී; මාර්ඩර් කේ. එස්. (2009). "Clinical measurement of mobility and balance impairments in Huntington's disease: validity and responsiveness". Gait & Posture. 29 (3): 433–6. doi:10.1016/j.gaitpost.2008.11.002. PMID 19111470. සම්ප්රවේශය 14 අප්රේල් 2009.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ "Unified Huntington's Disease Rating Scale (UHDRS)". UHDRS and Database. HSG. 1 පෙබරවාරි 2009. සම්ප්රවේශය 14 අප්රේල් 2009.
- ^ මයර්ස් ආර්. එච්. (2004). "Huntington's Disease Genetics". NeuroRx. 1 (2): 255–62. doi:10.1602/neurorx.1.2.255. PMC 534940. PMID 15717026.
- ^ a b c d e f g [1] ඩි ඩියේ-ස්මල්ඩර්ස් සී ඊ; ඩි වර්ට් ජී එම්; ලියෙබර්ස් අයි; ටිබන් ඒ; එවර්ස්-කියබූම්ස් ජී. (2013). "Reproductive options for prospective parents in families with Huntington's disease: Clinical, psychological and ethical reflections". Human Reproduction Update. 19 (3): 304–315. doi:10.1093/humupd/dms058. PMID 23377865.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ෆොරස්ට් කීනන් කේ; සිම්ප්සන් එස් ඒ; මියඩ්සිබ්රොඩ්ස්කා ඉසෙඩ්; ඇලෙක්සැන්ඩර් ඩී ඒ; සෙම්පර් ජේ. (2013). "How do partners find out about the risk of Huntington's disease in couple relationships?". Journal of Genetic Counseling. 22 (3): 336–44. doi:10.1007/s10897-012-9562-2. PMID 23297124.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ අර්වින් සී., විලියම්ස් ජේ. කේ., ජුහ්ල් ඒ. ආර්., මෙන්ජලිං එම්., මිල්ස් ජේ. ඒ., බොම්බේ වයි., හේඩ්න් එම්. ආර්., ක්වේඩ් කේ., ෂූල්සන් අයි., ටේලර් එස්., පල්සන් ජේ. එස්. (2010). "Perception, experience, and response to genetic discrimination in Huntington disease: the international RESPOND-HD study". American Journal of Medical Genetics Part B. 153B (5): 1081–93. doi:10.1002/ajmg.b.31079. PMC 3593716. PMID 20468061.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ බර්සන් සී. එම්., මාර්කි කේ. ආර්. (2001). "Genetic counseling issues in predictive genetic testing for familial adult-onset neurologic diseases". Semin Pediatr Neurol. 8 (3): 177–86. doi:10.1053/spen.2001.26451. PMID 11575847.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ස්මිත් ජේ. ඒ., අමිචී එස්., ස්ටීවන්සන් එම්., ක්වැරල් ඕ. (2002). "Risk Perception and Decision-making Processes in Candidates for Genetic Testing for Huntington's Disease: An Interpretative Phenomenological Analysis". Journal of Health Psychology. 7 (2): 131–44. doi:10.1177/1359105302007002398. PMID 22114233.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b හේඩ්න් එම්. ආර්. (මාර්තු 2003). "Predictive testing for Huntington's disease: a universal model?". Lancet Neurol. 2 (3): 141–2. doi:10.1016/S1474-4422(03)00317-X. PMID 12849232.
- ^ "Guidelines for the molecular genetics predictive test in Huntington's disease. International Huntington Association (IHA) and the World Federation of Neurology (WFN) Research Group on Huntington's Chorea". Neurology. 44 (8): 1533–6. 1994. doi:10.1212/WNL.44.8.1533. PMID 8058167.
- ^ ලෝස්කූට් එම්., වැන් බෙලූසන් එම්. ජේ., සෙනෙකා එස්., බවර් පී., ස්ටන්හවුස් එස්. ඒ., බාර්ටන් ඩී. ඊ. (2012). "EMQN/CMGS best practice guidelines for the molecular genetic testing of Huntington disease". Eur J Hum Genet. Online first (5): 480–6. doi:10.1038/ejhg.2012.200. PMC 3641377. PMID 22990145.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ෂුල්මාන් ජේ. ඩී., බ්ලැක් එස්. එච්., හැන්ඩිසයිඩ් ඒ., නැන්ස් ඩබ්. ඊ. (1996). "Preimplantation genetic testing for Huntington disease and certain other dominantly inherited disorders". Clinical Genetics. 49 (2): 57–58. doi:10.1111/j.1399-0004.1996.tb04327.x. PMID 8740912.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ස්ටර්න් එච්. ජේ., හාර්ටන් ජී. එල්., සිසන් එම්. ඊ., ජෝන්ස් එස්. එල්., ෆැලන් එල්. ඒ., තොර්සල් එල්. පී., ජෙට්ලයිනර් එම්. ඊ., බ්ලැක් එස්. එච්., ෂුල්මන් ජේ. ඩී. (2002). "Non-disclosing preimplantation genetic diagnosis for Huntington disease". Prenatal Diagnosis. 22 (6): 503–507. doi:10.1002/pd.359. PMID 12116316.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ "Predictive Testing for Huntington's Disease". 2011. සම්ප්රවේශය 7 මැයි 2013.
- ^ කුලියව් ඒ, වර්ලින්ස්කි වයි (2005). "Preimplantation diagnosis: A realistic option for assisted reproduction and genetic practice". Curr. Opin. Obstet. Gynecol. 17 (2): 179–83. doi:10.1097/01.gco.0000162189.76349.c5. PMID 15758612.
{{cite journal}}: Vancouver style error: name in name 1 (help) - ^ "Guidelines for Genetic Testing for Huntington's Disease". Heredity Disease Foundation. සම්ප්රවේශය 7 මැයි 2013.
- ^ a b ෂ්නයිඩර් එස්. ඒ., වෝකර් ආර්. එච්., භාටියා කේ. පී. (2007). "The Huntington's disease-like syndromes: what to consider in patients with a negative Huntington's disease gene test". Nat Clin Pract Neurol. 3 (9): 517–25. doi:10.1038/ncpneuro0606. PMID 17805246.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ෆ්රෑන්ක් එස්., ජැන්කොවික් ජේ. (2010). "Advances in the Pharmacological Management of Huntington's Disease". Drugs. 70 (5): 561–71. doi:10.2165/11534430-000000000-00000. PMID 20329804.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b c d e f වෝකර් එෆ්. ඕ. (2007). "Huntington's disease". Lancet. 369 (9557): 218–28 [224]. doi:10.1016/S0140-6736(07)60111-1. PMID 17240289.
- ^ a b c බොනෙලි ආර්. එම්., වෙනිං ජී. කේ., කැප්ෆැමර් එච්. පී. (2004). "Huntington's disease: present treatments and future therapeutic modalities". Int Clin Psychopharmacol. 19 (2): 51–62. doi:10.1097/00004850-200403000-00001. PMID 15076012. සම්ප්රවේශය 1 අප්රේල් 2009.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ලී, සී. එෆ්.; චර්න්, වයි. (2014). "Adenosine receptors and Huntington's disease". International review of neurobiology. 119: 195–232. doi:10.1016/B978-0-12-801022-8.00010-6. PMID 25175968.
- ^ සයිමොනින්, සී.; ඩුරු, සී.; සැලරොන්, ජේ.; හින්කර්, පී.; චාල්ස්, පී.; දේල්වාල්, ඒ.; යූසොව්, කේ.; බර්නෝෆ්, එස්.; අසුලේ, ජේ. පී.; වර්නි, සී.; ෂරර්, සී.; ට්රැන්චන්ට්, සී.; ගොයිසට්, සී.; ඩිබ්රෂලස්, එස්.; ඩිෆෙබ්වර්, එල්.; සැබ්ලොනියර්, බී.; රෝමන්-රූසොක්ස්, එම්.; බූයි, එල්.; ඩෙස්ටී, ඒ.; ගොඩෙෆ්රොයි, ඕ.; ඩ්යූර්, ඒ.; ලෑන්ඩ්වෙහර්මයර්, බී.; REGISTRY Study of the European Huntington's Disease, Network; බේචේඩ්-ලෙවි, ඒ. සී.; රිචඩ්, එෆ්.; බ්ලම්, ඩී.; ක්රිස්ට්කෝවියැක්, පී.; Huntington French Speaking, Network (ඔක්තෝබර් 2013). "Association between caffeine intake and age at onset in Huntington's disease". Neurobiology of disease. 58: 179–82. doi:10.1016/j.nbd.2013.05.013. PMID 23732677.
- ^ "EBM: Levels of Evidence". Essential Evidence Plus. සම්ප්රවේශය 2012-02-23.
- ^ පැනජියෝටේකිස් පී. එච්., ඩිසැරියෝ ජේ. ඒ., හිල්ඩන් කේ., ඔගාරා එම්., ෆැං ජේ. සී. (2008). "DPEJ tube placement prevents aspiration pneumonia in high-risk patients". Nutr Clin Pract. 23 (2): 172–5. doi:10.1177/0884533608314537. PMID 18390785.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b "EHDN Physiotherapy Guidance Document" (PDF). European HD Network Physiotherapy Working Group. සම්ප්රවේශය 2015-11-15.
- ^ ක්වින් එල්., බසී එම්. (February 2012). "Development of physiotherapy guidance and treatment-based classifications for people with Huntington's disease". Neurodegenerative Disease Management. 2 (1): 21–31. doi:10.2217/nmt.11.86.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ඛාලි එච්., ක්වින් එල්., වැන් ඩ්යුර්සන් ආර්., මාර්ටින් ආර්., රොසර් ඒ., බසී එම්. (ජනවාරි 2012). "Adherence to use of a home-based exercise DVD in people with Huntington disease: participants' perspectives". Physical Therapy. 92 (1): 69–82. doi:10.2522/ptj.20100438. PMID 21960468.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ "FDA Approves First Drug for Treatment of Chorea in Huntington's Disease". FDA Approves First Drug for Treatment of Chorea in Huntington's Disease. U.S. Food and Drug Administration. 15 අගෝස්තු 2008. සම්ප්රවේශය 10 අගෝස්තු 2008.
- ^ වෝකර් එෆ්. ඕ. (2007). "Huntington's disease". Lancet. 369 (9557): 218–28 [225]. doi:10.1016/S0140-6736(07)60111-1. PMID 17240289.
- ^ හාපර් පී. (2002). "Genetic counselling and presymptomatic testing". In බේට්ස් ජී., හාපර් පී., ජෝන්ස් එල්. (eds.). Huntington's Disease – තෙවන සංස්කරණය. Oxford: Oxford University Press. pp. 198–242. ISBN 0-19-851060-8.
{{cite book}}: Vancouver style error: punctuation in name 1 (help) - ^ හාපර් පී. එස්. (1999). "Huntington's disease: a clinical, genetic and molecular model for polyglutamine repeat disorders". Philos. Trans. R. Soc. Lond., B, Biol. Sci. 354 (1386): 957–6. doi:10.1098/rstb.1999.0446. PMC 1692597. PMID 10434293.
- ^ ඇන්ඩෲ එස්. ඊ., ගෝල්ඩ්බර්ග් වයි. පී., ක්රෙමර් බී., ටෙලේනියස් එච්., තයිල්මාන් ජේ., ඇඩම් එස්., ස්ටාර් ඊ., ස්ක්විටියරි එෆ්., ලින් බී., කැල්ච්මන් එම්. ඒ. (1993). "The relationship between trinucleotide (CAG) repeat length and clinical features of Huntington's disease". Nat. Genet. 4 (4): 398–403. doi:10.1038/ng0893-398. PMID 8401589.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ක්රෝෆර්ඩ් ඩී., ස්නෝඩ්න් ජේ. (2002). "Neuropyschological and neuropsychiatric aspects of Huntington's disease". In බේට්ස් ජී., හාපර් පී., ජෝන්ස් එල්. (eds.). Huntington's Disease – තෙවන සංස්කරණය. Oxford: Oxford University Press. pp. 62–87. ISBN 0-19-851060-8.
{{cite book}}: Vancouver style error: punctuation in name 1 (help) - ^ ඩි මේයෝ එල්., ස්ක්විටියරි එෆ්., නැපොලිටේනෝ ජී., කැම්පනෙලා ජී., ට්රොෆැටර් ජේ. ඒ., කෝර්නේලි පී. එම්. (1993). "Suicide risk in Huntington's disease". J. Med. Genet. 30 (4): 293–5. doi:10.1136/jmg.30.4.293. PMC 1016335. PMID 8487273.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b c d e f හාපර් පී. (2002). "The epidemiology of Huntington's disease". In බේට්ස් ජී., හාපර් පී., ජෝන්ස් එල්. (eds.). Huntington's Disease – තෙවන සංස්කරණය. Oxford: Oxford University Press. pp. 159–189. ISBN 0-19-851060-8.
{{cite book}}: Vancouver style error: punctuation in name 1 (help) - ^ ෂැරොන් අයි.; ෂැරොන් ආර්.; විල්කන්ස් ජේ. පී.; අර්සන් ටී. (2010). "Huntington Disease Dementia". emedicine, WebMD. Medscape. සම්ප්රවේශය 16 මැයි 2010.
- ^ ඩ්රයිවර්-ඩන්ක්ලි ඊ., කැවිනස් ජේ. එන්. (2007). "Huntington's disease". In Schapira AHV (ed.). Neurology and Clinical Neuroscience. Mosby Elsevier. pp. 879–885. ISBN 978-0-323-03354-1.
{{cite book}}: Vancouver style error: punctuation in name 1 (help) - ^ එවන්ස් එස්. ජේ., ඩග්ලස් අයි., රෝලින්ස් එම්. ඩී., වෙක්ස්ලර් එන්. එස්., ටැබ්රිසි එස්. ජේ., ස්මීත් එල්. (2013). "Prevalence of adult Huntington's disease in the UK based on diagnoses recorded in general practice records". Journal of Neurology, Neurosurgery, and Psychiatry. 84 (10): 1156–60. doi:10.1136/jnnp-2012-304636. PMC 3786631. PMID 23482661.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ඇවිලා-ගිරූ ආර්. (1973). "Medical and Social Aspects of Huntington's chorea in the state of Zulia, Venezuela". Advances in Neurology. 1: 261–6. ISSN 0091-3952. NAID 10021247802.
- ^ a b ගසෙලා ජේ. එෆ්., වෙක්ස්ලර් එන්. එස්., කෝනෙලි පී. එම්., නේලර් එස්. එල්., ඇන්ඩර්සන් එම්. ඒ., ටැන්සි ආර්. ඊ., වොට්කින්ස් පී. සී., ඔටිනා කේ., වොලස් එම්. ආර්., සකගුචි ඒ. වයි. (1983). "A polymorphic DNA marker genetically linked to Huntington's disease". Nature. 306 (5940): 234–8. doi:10.1038/306234a0. PMID 6316146.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ස්ක්විටියරි එෆ්., ඇන්ඩෲ එස්. ඊ., ගෝල්ඩ්බර්ග් වයි. පී. (1994). "DNA haplotype analysis of Huntington disease reveals clues to the origins and mechanisms of CAG expansion and reasons for geographic variations of prevalence". Hum. Mol. Genet. 3 (12): 2103–14. doi:10.1093/hmg/3.12.2103. PMID 7881406.
{{cite journal}}: Invalid|display-authors=ඇතුළු පිරිස(help); Vancouver style error: punctuation in name 1 (help) - ^ ස්වයින්සන්, ඕ (ජූලි 2012). "An Unusually Low Prevalence of Huntington's Disease in Iceland". European Neurology. 68: 48–51. doi:10.1159/000337680. PMID 22722209.
- ^ සිපිලා, ජුසි ඕ. ටී.; හියෙටලා, මර්ජා; සීටොනන්, අරි; පායිවරින්ටා, මාර්කු; මජාමා, කාරි (ජනවාරි 2015). "Epidemiology of Huntington's disease in Finland". Parkinsonism & Related Disorders. 21 (1): 46–49. doi:10.1016/j.parkreldis.2014.10.025. ISSN 1873-5126. PMID 25466405.
- ^ ඇග්ම්ක්විස්ට් ඊ. ඩබ්., එල්ටර්මන් ඩී. එස්., මැක්ලියොඩ් පී. එම්., හේඩ්න් එම්. ආර්. (2001). "High incidence rate and absent family histories in one quarter of patients newly diagnosed with Huntington disease in British Columbia". Clin. Genet. 60 (3): 198–205. doi:10.1034/j.1399-0004.2001.600305.x. PMID 11595021.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b හන්ටිංටන් ජී. (1872). "On Chorea". Medical and Surgical Reporter of Philadelphia. 26 (15). The Hague: Nijhoff: 317–321. ISBN 90-6186-011-3. සම්ප්රවේශය 1 අප්රේල් 2009.
- ^ කැරන් බෙලනිර්, ed. (2004). "Huntington Disease". Genetic Disorders Sourcebook (3වන ed.). Detroit: Omnigraphics. pp. 159–179. ISBN 0-7808-0742-1.
- ^ a b c d e f g h i j හාපර් පී. (2002). "Huntington's disease: a historical background". In බේට්ස් ජී., හාපර් පී., ජෝන්ස් එල්. (eds.). Huntington's Disease – තෙවන සංස්කරණය. Oxford: Oxford University Press. pp. 3–24. ISBN 0-19-851060-8.
{{cite book}}: Vancouver style error: punctuation in name 1 (help) - ^ a b c d වෙක්ස්ලර් ඒ., වෙක්ස්ලර් එන්. (2008). The Woman Who Walked Into the Sea. Huntington's and the Making of a Genetic Disease. Yale University Press. p. 288. ISBN 978-0-300-10502-5. සම්ප්රවේශය 2015-11-15.
{{cite book}}: Vancouver style error: punctuation in name 1 (help) - ^ ලුන්ඩ් ජේ. සී. (1860). "Chorea Sti Viti i Sætersdalen. Uddrag af Distriktslæge J. C. Lunds Medicinalberetning for 1860". Beretning om Sundhedstilstanden. Norway: 137–138.
- ^ ලැන්ස්තා ඩී. ජේ. (2000). "George Huntington (1850–1916) and hereditary chorea". J Hist Neurosci. 9 (1): 76–89. doi:10.1076/0964-704X(200004)9:1;1-2;FT076. PMID 11232352.
- ^ බ්රෝඩි අයි. ඒ., විල්කින්ස් ආර්. එච්. (1967). "Huntington's Chorea". Arch Neurol. 17 (3): 331. doi:10.1001/archneur.1967.00470270109013. PMID 4228262.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ජෙලිෆ් රස්. ඊ., මන්සී ඊ. බී., ඩෙවන්පෝර්ට් සී. බී. (1913). "Huntington's Chorea: A Study in Heredity". The Journal of Nervous and Mental Disease. 40 (12): 796–799. doi:10.1097/00005053-191312000-00010.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b ඩේවන්පෝට් සී. බී., මන්සී ඊ. බී. (1916). "Huntington's chorea in relation to heredity and eugenics". American Journal of Insanity. 73 (2): 195–222. doi:10.1176/appi.ajp.73.2.195.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ වෙසී පී. ආර්. (1932). "On the transmission of Huntington's chorea for 300 years – the Bures family group". Nervous and Mental Disease. 76 (6). Baltimore: 553–573. doi:10.1097/00005053-193212000-00001. සම්ප්රවේශය 1 අප්රේල් 2009.
- ^ a b වෙක්ස්ලර් ඒ. ආර්. (2002). "Chorea and community in a 19th-century town". Bull Hist Med. 76 (3): 495–527. doi:10.1353/bhm.2002.0150. PMID 12486915.
- ^ කොනේලි පී. එම්. (1984). "Huntington disease: genetics and epidemiology". Am. J. Hum. Genet. 36 (3): 506–26. PMC 1684448. PMID 6233902.
- ^ Wexler NS (2012) Huntington's Disease: Advocacy driving science. Annu Rev Med 63:1–22
- ^ "The Venezuela Huntington's disease project". Hereditary Disease Foundation website. Hereditary Disease Foundation. 2008. සම්ප්රවේශය 8 September 2008.
- ^ a b මැක්ඩොනල්ඩ් එම්. (1993). "A novel gene containing a trinucleotide repeat that is expanded and unstable on Huntington's disease chromosomes. The Huntington's Disease Collaborative Research Group". Cell. 72 (6): 971–83. doi:10.1016/0092-8674(93)90585-E. PMID 8458085.
- ^ බර්ට්රම් එල්., ටැන්සි ආර්. ඊ. (2005). "The genetic epidemiology of neurodegenerative disease". J. Clin. Invest. 115 (6): 1449–57. doi:10.1172/JCI24761. PMC 1137006. PMID 15931380.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ ලා ස්පැන්ඩා ඒ. ආර්., රොලිං ඩී. බී., හාර්ඩිං ඒ. ඊ. (1992). "Meiotic stability and genotype-phenotype correlation of the trinucleotide repeat in X-linked spinal and bulbar muscular atrophy". Nat. Genet. 2 (4): 301–4. doi:10.1038/ng1292-301. PMID 1303283.
{{cite journal}}: Invalid|display-authors=ඇතුළු පිරිස(help); Vancouver style error: punctuation in name 1 (help) - ^ a b c රොස් සී. ඒ., ටැබ්රිසි එස්. ජේ. (ජනවාරි 2011). "Huntington's disease: from molecular pathogenesis to clinical treatment". Lancet neurology. 10 (1): 83–98. doi:10.1016/S1474-4422(10)70245-3. PMID 21163446.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ "What is HD?". Huntington's disease association. සම්ප්රවේශය 18 දෙසැම්බර් 2011.
- ^ ඩේවන්පෝට් සී. බී. (1915). "Huntington's Chorea in Relation to Heredity and Eugenics". Proc. Natl. Acad. Sci. U.S.A. 1 (5): 283–5. doi:10.1073/pnas.1.5.283. PMC 1090803. PMID 16575999.
- ^ රොලින් බී. ඊ. (2006). "The Regulation of Animal Research and the Emergence of Animal Ethics: A Conceptual History". Theoretical Medicine and Bioethics. 27 (4): 285–304. doi:10.1007/s11017-006-9007-8. PMID 16937023.
- ^ ඩොවර්ෆ්ලිංගර් ආර්. එම්. (2008). "The problem of deception in embryonic stem cell research". Cell Prolif. 41 Suppl 1: 65–70. doi:10.1111/j.1365-2184.2008.00492.x. PMID 18181947.
- ^ චැප්මන් එම්. ඒ. (1990). "Predictive testing for adult-onset genetic disease: ethical and legal implications of the use of linkage analysis for Huntington disease". Am. J. Hum. Genet. 47 (1): 1–3. PMC 1683745. PMID 2140926.
- ^ හගින්ස් එම්., බ්ලොච් එම්., කනානි එස්. (1990). "Ethical and legal dilemmas arising during predictive testing for adult-onset disease: the experience of Huntington disease". Am. J. Hum. Genet. 47 (1): 4–12. PMC 1683755. PMID 1971997.
{{cite journal}}: Invalid|display-authors=ඇතුළු පිරිස(help); Vancouver style error: punctuation in name 1 (help) - ^ "Insurance Genetics Moratorium extended to 2017" (Press release). Association of British Insurers. 5 අප්රේල් 2011. 2016-03-04 දින මුල් පිටපත වෙතින් සංරක්ෂණය කරන ලදී. සම්ප්රවේශය 13 ජනවාරි 2016.
- ^ "Expert backs gene test disclosure". BBC article. 7 June 2007.
- ^ බිනෙඩෙල් ජේ., සොල්ඩන් ජේ. ආර්., ස්කෝර්ෆීල්ඩ් ජේ., හාපර් පී. එස්. (1996). "Huntington's disease predictive testing: the case for an assessment approach to requests from adolescents". J. Med. Genet. 33 (11): 912–8. doi:10.1136/jmg.33.11.912. PMC 1050784. PMID 8950670.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ බොරි පී., ගොෆින් ටී., නයිස් එච්., ඩියරික්ස් කේ. (2008). "Predictive genetic testing in minors for adult-onset genetic diseases". Mt. Sinai J. Med. 75 (3): 287–96. doi:10.1002/msj.20038. PMID 18704981.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ a b c බ්රෝඩ් පී. ආර්., ඩි වර්ට් ජී. එම්., එවර්ස්-කියබූම්ස් ජී., පෙටිගෲ ආර්. ඒ., ජෙරාඩ්ස් ජේ. පී. (1998). "Non-disclosure preimplantation genetic diagnosis for Huntington's disease: practical and ethical dilemmas". Prenat. Diagn. 18 (13): 1422–6. doi:10.1002/(SICI)1097-0223(199812)18:13<1422::AID-PD499>3.0.CO;2-R. PMID 9949442.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ "The International Huntington Association". International Huntington Association. 2013. සම්ප්රවේශය 3 අප්රේල් 2009.
- ^ "US Senate s. resolution 531". S. Res. 531. US Senate. 6 අප්රේල් 2008. සම්ප්රවේශය 10 අගෝස්තු 2008.
- ^ a b ඕඩ්ලිං-ස්මී එල්. (17 මැයි 2007). "Biomedical philanthropy: The money tree". Nature. 447 (7142): 251–251. doi:10.1038/447251a.
- ^ "CHDI Foundation, Inc". සම්ප්රවේශය 4 දෙසැම්බර් 2011.
- ^ චෙක් ඊ. (17 මැයි 2007). "Biomedical philanthropy: Love or money". Nature. 447 (7142): 252–253. doi:10.1038/447252a. PMID 17507955.
- ^ ටර්නර් සී., ෂැපිරා ඒ. එච්. (2010). "Mitochondrial matters of the brain: the role in Huntington's disease". Journal of bioenergetics and biomembranes. 42 (3): 193–8. doi:10.1007/s10863-010-9290-y. PMID 20480217.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ වයිල්ඩ්, ඊ. ජේ.; ටැබ්රිසි, එස්. ජේ. (15 September 2014). "Targets for future clinical trials in Huntington's disease: what's in the pipeline?". Movement disorders : official journal of the Movement Disorder Society. 29 (11): 1434–45. doi:10.1002/mds.26007. PMID 25155142.
- ^ a b මුනෝස්-සන්ජුවාන්, අයි.; බේට්ස්, ජී. පී. (2011). "The importance of integrating basic and clinical research toward the development of new therapies for Huntington disease". Journal of Clinical Investigation. 121 (2): 476–483. doi:10.1172/JCI45364. PMC 3026740. PMID 21285520.
- ^ මැක්බ්රයිඩ්, ජෝඩි එල්.; පිට්සර්, මාක් ආර්.; බෞඩෲ, රයන් එල්.; ඩූෆර්, බ්රෙට්; හොබ්ස්, තියඩෝර්; ඔජේඩා, සර්ජියෝ ආර්.; ඩේවිඩ්සන්, බෙවර්ලි එල්. (25 ඔක්තෝබර් 2011). "Preclinical Safety of RNAi-Mediated HTT Suppression in the Rhesus Macaque as a Potential Therapy for Huntington's Disease". Molecular Therapy. 19 (12): 2152–2162. doi:10.1038/mt.2011.219. PMC 3242667. PMID 22031240.
- ^ කොර්ඩසියවික්ස්, හොලී බී.; ස්ටැනෙක්, ලීසා එම්.; වැන්ක්වික්ස්, එඩ්වඩ් වී.; මේසර්, කර්ට්; මැක්ඇලෝනිස්, මලිසා එම්.; පයිටල්, කිම්බර්ලි ඒ.; ආර්ටේටස්, ජොනතන් ඩබ්.; වෙයිස්, ඇන්ඩ්රියස්; සෙං එච්. චෙං; ෂිහාබුද්දීන්, ලම්යා එස්.; හුං, ජිනී; බෙනට්, සී. ෆ්රෑන්ක්; ක්ලේව්ලන්ඩ්, ඩොන් ඩබ්. (21 June 2012). "Sustained Therapeutic Reversal of Huntington's Disease by Transient Repression of Huntingtin Synthesis". Neuron. 74 (6): 1031–1044. doi:10.1016/j.neuron.2012.05.009.
{{cite journal}}: no-break space character in|first=at position 5 (help) - ^ බාර්නිස්, ඩී. ඩබ්.; විට්ලි, ආර්. ජේ. (පෙබරවාරි 1987). "Antiviral therapy and pulmonary disease". Chest. 91 (2): 246–51. doi:10.1172/JCI45130. PMID 3026739.
- ^ "Landmark Huntington's trial starts". සම්ප්රවේශය 19 ඔක්තෝබර් 2015.
- ^ "Safety, Tolerability, Pharmacokinetics, and Pharmacodynamics of IONIS-HTTRx in Patients With Early Manifest Huntington's Disease - Full Text View - ClinicalTrials.gov". clinicaltrials.gov. සම්ප්රවේශය 18 අප්රේල් 2016.
- ^ වයිල්ඩ්, ඊ. ජේ.; බොගියෝ, ආර්.; ලැන්ග්බෙන්, ඩී.; රොබට්සන්, එන්.; හේඩර්, එස්.; මිලර්, ජේ. ආර්.; සෙටර්බර්ග්, එච්.; ලීවිට්, බී. ආර්.; කූන්, ආර්.; ටැබ්රිසි, එස්. ජේ.; මැක්ඩොනල්ඩ්, ඩී.; වෙයිස්, ඒ. (May2015). "Quantification of mutant huntingtin protein in cerebrospinal fluid from Huntington's disease patients". The Journal of Clinical Investigation. 125 (5): 1979–86. doi:10.1172/jci80743. PMC 4463213. PMID 25844897.
{{cite journal}}: Check date values in:|date=(help) - ^ චේස්, ඇලෙක්ස් (21 අප්රේල් 2015). "Huntington disease: Cerebrospinal fluid and MRI biomarkers for prodromal HD". Nature Reviews Neurology. 11 (5): 245–245. doi:10.1038/nrneurol.2015.63.
- ^ කයිසර්, මේගන් එස්.; කොර්ඩසියෙවික්ස්, හොලී බී.; මැක්බ්රයිඩ්, ජෝඩි එල්. (15 අප්රේල් 2016). "Gene suppression strategies for dominantly inherited neurodegenerative diseases: lessons from Huntington's disease and spinocerebellar ataxia". Human Molecular Genetics. 25 (R1): R53–R64. doi:10.1093/hmg/ddv442.
- ^ ක්ලෙලන්ඩ් සී. ඩී., බාකර් ආර්. ඒ., වොට්ස් සී. (2008). "Cell therapy in Huntington disease". Neurosurg Focus. 24 (3–4): E9. doi:10.3171/FOC/2008/24/3-4/E8. PMID 18341412.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ කන්ඩිෆ් පී. ඊ., ඇන්ඩර්සන් එස්. ඒ. (31 මැයි 2011). "Impact of induced pluripotent stem cells on the study of central nervous system disease". Current Opinion in Genetics & Development. 21 (3): 354–361. doi:10.1016/j.gde.2011.01.008. PMID 21277194.
{{cite journal}}: Vancouver style error: punctuation in name 1 (help) - ^ වයිල්ඩ්, ඊ. ජේ.; ටැබ්රිසි, එස්. ජේ. (15 සැප්තැම්බර් 2014). "Targets for future clinical trials in Huntington's disease: what's in the pipeline?". Movement disorders : official journal of the Movement Disorder Society. 29 (11): 1434–45. doi:10.1002/mds.26007. PMID 25155142.
- ^ "Completed Clinical Trials". Huntington Study Group. 28 ජූනි 2012 දින මුල් පිටපත වෙතින් සංරක්ෂණය කරන ලදී. සම්ප්රවේශය 4 පෙබරවාරි 2012.
බාහිර සබැඳි
[සංස්කරණය] හන්ටිංටන්ගේ රෝගය ගැන තවත් දේ විකිපිඩියා සහෝදර ව්යාපෘති හරහා සොයාගන්න
| |
| වික්ෂනරිය වෙතින් අර්ථ දැක්වීම් | |
| කොමන්ස් වෙතින් ඡායාරූප හා මාධ්ය | |
| විකිසරසවිය වෙතින් ඉගෙනුම් මූලාශ්ර | |
| විකිපුවත් වෙතින් පුවත් කථාංග | |
| විකිප්රභව වෙතින් ප්රභව පෙළ | |
| විකිපොත් වෙතින් පෙළපොත් | |
- හන්ටිංටන්ගේ රෝගය at the Open Directory Project
 විකිමූලාශ්ර සතුව මෙම ලිපියට අදාල මුල් පිටපත පවතී: කෝරියාව පිළිබඳ
විකිමූලාශ්ර සතුව මෙම ලිපියට අදාල මුල් පිටපත පවතී: කෝරියාව පිළිබඳ- HOPES ව්යාපෘතිය සංරක්ෂණය කළ පිටපත 2020-08-27 at the Wayback Machine – ස්ටැන්ෆර්ඩ් විශ්වවිද්යාලයේ HD තොරතුරු ව්යාපෘතිය
- HDBuzz – සරල බසින් විද්යාඥයින් විසින් ලියන ලද HD පර්යේෂණ පුවත්
- HD Drug Works – වර්තමාන ප්රතිකාර සහ සැලසුම් කළ අත්හදා බැලීම් පිළිබඳ පුවත්
