pH දර්ශකය
pH දර්ශකයක් යනු ද්රාවණයකට කුඩා ප්රමාණවලින් එකතු කරන හලෝක්රොමික් රසායනික සංයෝගයකි, එබැවින් ද්රාවණයේ pH ( ආම්ලිකතාව ය හෝ මූලිකත්වය ) අවශෝෂණ සහ/හෝ විමෝචන ගුණාංගවල වෙනස් වීම් මගින් දෘශ්ය හෝ වර්ණාවලීක්ෂව තීරණය කළ හැක. එබැවින්, pH දර්ශකය යනු Arrhenius ආකෘතියේ හයිඩ්රෝනියම් අයන (H 3 O + ) හෝ හයිඩ්රජන් අයන (H + ) සඳහා රසායනික අනාවරණයකි. සාමාන්යයෙන්, දර්ශකය pH අගය අනුව විසඳුමේ වර්ණය වෙනස් කිරීමට හේතු වේ. දර්ශක වෙනත් භෞතික ගුණාංගවල වෙනසක් ද පෙන්විය හැක; උදාහරණයක් ලෙස, ආඝ්රාණ දර්ශක ඔවුන්ගේ සුවඳෙහි වෙනසක් පෙන්නුම් කරයි. උදා සීන ද්රාවණයක pH අගය 25°C දී 7.0 වේ ( සම්මත රසායනාගාර තත්ව ). 7.0 ට අඩු pH අගයක් සහිත විසඳුම් ආම්ලික ලෙස සලකනු ලබන අතර 7.0 ට වැඩි pH අගය සහිත විසඳුම් මූලික වේ. බොහෝ ස්වාභාවික ඇති කාබනික සංයෝග කාබොක්සිලික් අම්ල සහ ඇමයින් වැනි දුර්වල ඉලෙක්ට්රොලයිට් වන බැවින් pH දර්ශක ජීව විද්යාවේ සහ විශ්ලේෂණ රසායන විද්යාවේ බොහෝ යෙදුම් සොයා ගනී. එපමණක් නොව, pH දර්ශක රසායනික විශ්ලේෂණයේ දී භාවිතා කරන ප්රධාන දර්ශක සංයෝග තුනෙන් එකකි. ලෝභ කැටායනවල ප්රමාණාත්මක විශ්ලේෂණය සඳහා, සංකීර්ණමිතික දර්ශක භාවිතය වඩාත් ප්රිය කරයි, [1] [2] තුන් වන සංයෝග පන්තිය, රෙඩොක්ස් දර්ශක, රෙඩොක්ස් ටයිටරේෂන් (රසායනික රෙඩොක්ස් ප්රතික්රියා එකක් හෝ වැඩි ගණනක් ඇතුළත් රෙඩොක්ස් ප්රතික්රියා වල පදනම ලෙස භාවිතා කරයි. විශ්ලේෂණය).
න්යාය
[සංස්කරණය]ඔවුන් තුළ ම, pH දර්ශක සාමාන්යයෙන් දුර්වල අම්ල හෝ දුර්වල භෂ්ම වේ. ජලීය ද්රාවණවල ආම්ලික pH දර්ශකවල සාමාන්ය ප්රතික්රියා යෝජනා ක්රමය මෙසේ සකස් කළ හැක:
- HInd (aq) + H2O</br> H2O (l) ⇌ H3O+</br> H3O+ (aq) + Ind− (aq)
එහි දී, "HInd" යනු ආම්ලික ස්වරූපය සහ "Ind - " දර්ශකයේ සංයුජ පාදය සඳහා වේ. ජලීය ද්රාවණවල මූලික pH දර්ශක සඳහා ප්රතිවිරුද්ධ ව:
- IndOH (aq) + H2O</br> H2O (l) ⇌ H2O</br> H2O (l) + Ind+ (aq) + OH− (aq)
මෙහි "IndOH" යන්නෙන් මූලික ස්වරූපය සහ "Ind + " යනු දර්ශකයේ සංයුජ අම්ලය වේ.
ආම්ලික/මූලික දර්ශකයේ සාන්ද්රණයට සංයුජ අම්ල/පාදයේ සාන්ද්රණයේ අනුපාතය ද්රාවණයේ pH (හෝ pOH) තීරණය කරන අතර වර්ණය pH අගයට (හෝ pOH) සම්බන්ධ කරයි. දුර්වල විද්යුත් විච්ඡේදන pH දර්ශක සඳහා, Henderson-Hasselbalch සමීකරණය මෙසේ ලිවිය හැකිය:
- pH = p K a + log <sub id="mwUg">10</sub>
- pOH = p K b + log 10
ආම්ලිකතා නියතයෙන් සහ මූලිකතා නියතයෙන් ව්යුත්පන්න වූ සමීකරණවල සඳහන් වන්නේ pH අගය දර්ශකයේ p K a හෝ p K b අගයට සමාන වන විට විශේෂ දෙක ම 1:1 අනුපාතයකින් පවතින බවයි. pH අගය p K a හෝ p K b අගයට වඩා වැඩි නම්, සංයුජ පාදයේ සාන්ද්රණය අම්ලයේ සාන්ද්රණයට වඩා වැඩි වන අතර සංයුජ පාදය හා සම්බන්ධ වර්ණය ආධිපත්යය දරයි. pH අගය p K a හෝ p K b අගයට වඩා අඩු නම්, ප්රතිලෝම ය සත්ය වේ.
සාමාන්යයෙන්, p K a හෝ p K b අගයේ දී වර්ණ වෙනස් වීම ක්ෂණිකව සිදු නොවේ, නමුත් වර්ණ මිශ්රණයක් පවතින ස්ථානයේ pH පරාසයක් පවතී. මෙම pH අගය දර්ශක අතර වෙනස් වේ, නමුත් රීතියක් ලෙස, එය p K a හෝ p K b අගය ප්ලස් හෝ ඍණ එක අතර වැටේ. මෙය උපකල්පනය කරන්නේ අවම වශයෙන් අනෙකුත් විශේෂවලින් 10% ක් පවතින තාක් කල් විසඳුම් ඒවායේ වර්ණය රඳවා තබා ගන්නා බවයි. උදාහරණයක් ලෙස, සංයුජ පාදයේ සාන්ද්රණය අම්ලයේ සාන්ද්රණයට වඩා 10 ගුණයකින් වැඩි නම්, ඒවායේ අනුපාතය 10:1 වන අතර, ඒ අනුව pH අගය p K a වේ. + 1 හෝ p K b + 1. ප්රතිවිරුද්ධ ව, පාදයට සාපේක්ෂව අම්ලයේ 10 ගුණයක අතිරික්තයක් සිදුවුවහොත්, අනුපාතය 1:10 වන අතර pH අගය p K a වේ. - 1 හෝ p K b - 1.
ප්රශස්ත නිරවද්යතාව ය සඳහා, විශේෂ දෙක අතර වර්ණ වෙනස හැකි තාක් පැහැදිලි විය යුතු අතර, වර්ණයෙහි pH පරාසය පටු වන තරමට වඩා හොඳ ය. phenolphthalein වැනි සමහර දර්ශකවල, එක් විශේෂයක් අවර්ණ වන අතර, මෙතිල් රතු වැනි අනෙකුත් දර්ශකවල, විශේෂ දෙක ම වර්ණයක් ලබා දෙයි. pH දර්ශක ඔවුන්ගේ නම් කරන ලද pH පරාසය තුළ කාර්යක්ෂමව ක්රියා කරන අතර, අනවශ්ය අතුරු ප්රතික්රියා හේතුවෙන් ඒවා සාමාන්යයෙන් pH පරිමාණයේ අන්තයේ දී විනාශ වේ.
අයදුම්පත
[සංස්කරණය]
රසායනික ප්රතික්රියාවක ප්රමාණය තීරණය කිරීම සඳහා විශ්ලේෂණාත්මක රසායන විද්යාවේ සහ ජීව විද්යාවේ ටයිටරේෂන්වල pH දර්ශක නිතර භාවිතා වේ. වර්ණවල ආත්මීය තේරීම (නිර්ණය) නිසා, pH දර්ශක අපැහැදිලි කියවීම් වලට ගොදුරු වේ. pH අගය නිවැරදිව මැනීමට අවශ්ය යෙදුම් සඳහා, pH මීටරයක් නිතර භාවිතා වේ. සමහර විට, pH අගයන්ට පුළුල් පරාසයක සුමට වර්ණ වෙනස්කම් කිහිපයක් ලබා ගැනීම සඳහා විවිධ දර්ශකවල සම්මිශ්රණයක් භාවිතා වේ. මෙම වාණිජ දර්ශක (උදා, විශ්ව දර්ශක සහ හයිඩ්රියන් පත්රිකා ) භාවිතා කරනු යේ pH අගය පිළිබඳ දළ දැනුමක් අවශ්ය විට පමණි.
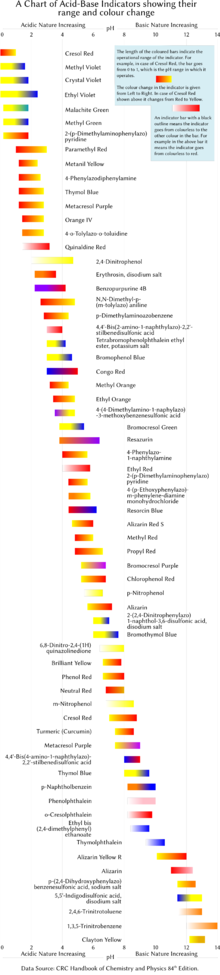
පහත වගුවේ දක්වා ඇත්තේ පොදු රසායනාගාර pH දර්ශක කිහිපයක් වේ. දර්ශක සාමාන්යයෙන් ලැයිස්තු ගත සංක්රාන්ති පරාසය තුළ pH අගයන්හි අතරමැදි වර්ණ පෙන්වයි. උදාහරණයක් ලෙස, phenol රතු pH 6.8 සහ pH 8.4 අතර තැඹිලි පැහැයක් දක්වයි. විසඳුමේ දර්ශකයේ සාන්ද්රණය සහ එය භාවිතා කරන උෂ්ණත්වය මත සංක්රාන්ති පරාසය තරමක් වෙනස් විය හැක. දකුණු පස ඇති රූපය ඔවුන්ගේ මෙහෙයුම් පරාසය සහ වර්ණ වෙනස්කම් සමඟ දර්ශක පෙන්වයි.
| Indicator | Low pH color | Transition low end |
Transition high end |
High pH color |
|---|---|---|---|---|
| Gentian violet (Methyl violet 10B) | yellow | 0.0 | 2.0 | blue-violet |
| Malachite green (first transition) | yellow | 0.0 | 2.0 | green |
| Malachite green (second transition) | green | 11.6 | 14.0 | colorless |
| Thymol blue (first transition) | red | 1.2 | 2.8 | yellow |
| Thymol blue (second transition) | yellow | 8.0 | 9.6 | blue |
| Methyl yellow | red | 2.9 | 4.0 | yellow |
| Methylene blue | colorless | 5.0 | 9.0 | dark blue |
| Bromophenol blue | yellow | 3.0 | 4.6 | blue |
| Congo red | blue-violet | 3.0 | 5.0 | red |
| Methyl orange | red | 3.1 | 4.4 | yellow |
| Screened methyl orange (first transition) | red | 0.0 | 3.2 | purple-grey |
| Screened methyl orange (second transition) | purple-grey | 3.2 | 4.2 | green |
| Bromocresol green | yellow | 3.8 | 5.4 | blue |
| Methyl red | red | 4.4 | 6.2 | yellow |
| Methyl purple | purple | 4.8 | 5.4 | green |
| Azolitmin (litmus) | red | 4.5 | 8.3 | blue |
| Bromocresol purple | yellow | 5.2 | 6.8 | purple |
| Bromothymol blue | yellow | 6.0 | 7.6 | blue |
| Phenol red | yellow | 6.4 | 8.0 | red |
| Neutral red | red | 6.8 | 8.0 | yellow |
| Naphtholphthalein | pale red | 7.3 | 8.7 | greenish-blue |
| Cresol red | yellow | 7.2 | 8.8 | reddish-purple |
| Cresolphthalein | colorless | 8.2 | 9.8 | purple |
| Phenolphthalein (first transition) | colorless | 8.3 | 10.0 | purple-pink |
| Phenolphthalein (second transition) | purple-pink | 12.0 | 13.0 | colorless |
| Thymolphthalein | colorless | 9.3 | 10.5 | blue |
| Alizarine Yellow R | yellow | 10.2 | 12.0 | red |
| Indigo carmine | blue | 11.4 | 13.0 | yellow |
විශ්ව දර්ශකය
[සංස්කරණය]| pH පරාසය | විස්තර | වර්ණ |
|---|---|---|
| 1-3 | ශක්තිමත් අම්ලය | රතු |
| 3 - 6 | දුර්වල අම්ලය | තැඹිලි/කහ |
| 7 | මධ්යස්ථ | හරිත |
| 8 - 11 | දුර්වල ක්ෂාර | නිල් |
| 11-14 | ශක්තිමත් ක්ෂාර | වයලට්/ඉන්ඩිගෝ |
නිවැරදි pH අගය මැනීම
[සංස්කරණය]
තරංග ආයා ම දෙකකින් හෝ වැඩි ගණනකින් අවශෝෂණය ප්රමාණාත්මක ව මැනීම මගින් pH අගය ඉතා නිවැරදි මිනුම් ලබා ගැනීමට දර්ශකයක් භාවිතා කළ හැක. H + සහ A − ලෙස විඝටනය වන සරල අම්ලයක් වන HA ලෙස දර්ශකය ලබා ගැනීමෙන් මූලධර්මය නිදර්ශනය කළ හැක.
- HA ⇌ H + + A -
අම්ල විඝටන නියතයේ අගය, p K a, දැන ගත යුතු ය. λ x සහ λ y තරංග ආයාමයේදී HA සහ A - විශේෂ දෙකේ ε HA සහ ε A - ද පෙර අත්හදා බැලීම් මගින් තීරණය කර තිබිය යුතු ය. බියර් ගේ නීතියට කීකරු විය යුතු යැයි උපකල්පනය කළ හොත්, තරංග ආයා ම දෙකෙහි මනින ලද අවශෝෂණ A x සහ A y සරල වම එක් එක් විශේෂය නිසා සිදු වන අවශෝෂණයන්හි එකතුව වේ.
මේවා [HA] සහ [A - ] සාන්ද්රණ දෙකෙහි සමීකරණ දෙකකි. විසඳූ පසු, pH අගය ලබා ගනී
තරංග ආයා ම දෙකකට වඩා මිනුම් සිදු කරන්නේ නම්, සාන්ද්රණය [HA] සහ [A - ] රේඛීය අවම කොටු වලින් ගණනය කළ හැක. ඇත්ත වශයෙන් ම, මේ සඳහා සම්පූර්ණ වර්ණාවලියක් භාවිතා කළ හැකිය. මෙම ක්රියාවලිය බ්රෝමොක්රෙසෝල් හරිත දර්ශකය සඳහා නිදර්ශනය කර ඇත. නිරීක්ෂණය කරන ලද වර්ණාවලිය (කොළ) යනු HA (රන්) සහ A - (නිල්) වර්ණාවලිවල එකතුව, විශේෂ දෙකේ සාන්ද්රණය සඳහා බරයි.
තනි දර්ශකයක් භාවිතා කරන විට, මෙම ක්රමය pH පරාසයේ මිනුම් වලට සීමා වේ p K a ± 1, නමුත් දර්ශක දෙකක හෝ වැඩි ගණනක මිශ්රණ භාවිතා කිරීමෙන් මෙම පරාසය දීර්ඝ කළ හැක. දර්ශකවල තීව්ර අවශෝෂණ වර්ණාවලි ඇති බැවින්, දර්ශක සාන්ද්රණය සාපේක්ෂව අඩු වන අතර, දර්ශකය ම pH අගයට නො සැලකිය හැකි බලපෑමක් ඇති කරයි.
සමානතා ලක්ෂ්යය
[සංස්කරණය]අම්ල-පාදක ටයිටරේෂන් වල දී, නොගැළපෙන pH දර්ශකයක් සැබෑ සමානතා ලක්ෂ්යයට පෙර හෝ පසුව දර්ශක අඩංගු ද්රාවණයේ වර්ණ වෙනසක් ඇති කරයි. ප්රතිඵලයක් වශයෙන්, භාවිතා කරන pH දර්ශකය මත පදනම් විසඳුමක් සඳහා විවිධ සමානතා ලක්ෂ්යයන් නිගමනය කළ හැක. මක්නිසාද යත්, දර්ශක අඩංගු විසඳුමේ සුළු වර්ණ වෙනසක් මගින් සමානතා ලක්ෂ්යයට ළඟා වී ඇති බව අඟවන බැවිනි. එබැවින්, වඩාත් සුදුසු pH දර්ශකයෙහි ඵලදායි pH පරාසයක් ඇත, එහි දී වර්ණය වෙනස් වීම පැහැදිලිව පෙනේ, එය ටයිටේට් කර ඇති ද්රාවණයේ සමානතා ලක්ෂ්යයේ pH අගය ආවරණය කරයි. [3]
ස්වාභාවික ව ඇති pH දර්ශක
[සංස්කරණය]බොහෝ ශාක හෝ ශාක කොටස් වල ස්වාභාවික ව වර්ණ ගැන්වූ ඇන්තොසියානින් පවුලේ සංයෝගවල රසායනික ද්රව්ය අඩංගු වේ. ඒවා ආම්ලික ද්රාවණවල රතු වන අතර මූලික වශයෙන් නිල් වේ. ඇන්තොසියානින් කොළ ( රතු ගෝවා ) ඇතුළු වර්ණවත් ශාක හා ශාක කොටස් රාශියකින් ජලය හෝ වෙනත් ද්රාවක සමඟ නිස්සාරණය කළ හැකිය; මල් ( ගෙරානියම්, පොපි හෝ රෝස පෙති); බෙරි ( බ්ලූබෙරීස්, බ්ලැක්කුරන්ට් ); සහ කඳන් ( රුබාබ් ). අමු pH දර්ශකයක් සෑදීම සඳහා ගෘහස්ථ ශාක වලින්, විශේෂයෙන් රතු ගෝවා වලින් ඇන්තොසියානින් නිස්සාරණය කිරීම ජනප්රිය හඳුන්වා දීමේ රසායන විද්යා නිරූපණයකි.
ලිට්මස්, මධ්ය කාලීන යුගයේ ඇල්කෙමිස්ට්වරුන් විසින් භාවිතා කරන ලද සහ තවමත් පහසුවෙන් ලබා ගත හැකි අතර, ලයි කන විශේෂවල, විශේෂයෙන් රොසෙල්ලා ටින්ක්ටෝරියා මිශ්රණයකින් සාදන ලද ස්වාභාවික ව ඇති pH දර්ශකයකි. ලිට්මස් යන වචනය වචනාර්ථයෙන් පැරණි නෝර්ස් භාෂාවෙන් 'වර්ණ පාසි' යන්නෙන් වේ ( ලීටර් බලන්න). අම්ල ද්රාවණවල රතු සහ ක්ෂාරවල නිල් අතර වර්ණය වෙනස් වේ. 'ලිට්මස් පරීක්ෂණය' යන යෙදුම විකල්ප අතර අධිකාරි ලෙස වෙන් කර හඳුනා ගැනීමට අදහස් කරන ඕනෑම පරීක්ෂණයක් සඳහා බහුලව භාවිතා වන රූපකයක් බවට පත්ව ඇත.
පාංශු ආම්ලිකතාව ය අනුව හයිඩ්රේන්ජා මැක්රොෆිලා මල් වර්ණය වෙනස් කළ හැකිය. අම්ල පසෙහි, පසෙහි රසායනික ප්රතික්රියා සිදු වන අතර එමගින් මෙම ශාක සඳහා ඇලුමිනියම් ලබා ගත හැකි අතර මල් නිල් පැහැයට හැරේ. ක්ෂාරීය පසෙහි, මෙම ප්රතික්රියා සිදු විය නො හැකි අතර එබැවින් ඇලුමිනියම් ශාකයට නො ගනී. එහි ප්රතිඵලයක් වශයෙන් මල් රෝස පැහැයෙන් පවතී.
තවත් ප්රයෝජනවත් ස්වභාවික pH දර්ශකය වන්නේ කුළුබඩු කහ . එය අම්ලවලට නිරාවරණය වන විට කහ පැහැයට හැරෙන අතර ක්ෂාරයක් ඇති විට රතු දුඹුරු පැහැයට හැරේ.
| දර්ශකය | අඩු pH වර්ණය | ඉහළ pH වර්ණය |
|---|---|---|
| Hydrangea මල් | නිල් | රෝස සිට දම් දක්වා |
| ඇන්තොසියානින් | රතු | නිල් |
| ලිට්මස් | රතු | නිල් |
| කහ | කහ | රතු පැහැයට හුරු දුඹුරු |
-
අම්ල පසෙහි හයිඩ්රේන්ජා
-
ක්ෂාරීය පසෙහි හයිඩ්රේන්ජා
-
රතු ගෝවා සාරය pH දර්ශකයේ අනුක්රමණයක් වම් පස ආම්ලික ද්රාවණයේ සිට දකුණේ මූලික දක්වා
-
ෙබ්කිං සෝඩා (වමේ) සහ විනාකිරි (දකුණේ) පොඟවා ඇති දම් පැහැති වට්ටක්කා. ඇන්තොසියානින් pH දර්ශකයක් ලෙස ක්රියා කරයි.
-
ජලයේ දියවන කහ ආම්ලිකතාවය යටතේ කහ සහ ක්ෂාරීය තත්ත්ව යටතේ රතු දුඹුරු වේ
- ^ . London. 1957. pp. 29–46.
{{cite book}}: Missing or empty|title=(help)CS1 maint: location missing publisher (link) - ^ . Poole, UK. 1969. pp. 14–82.
{{cite book}}: Missing or empty|title=(help)CS1 maint: location missing publisher (link) - ^ . New York. 2009. pp. 319–324.
{{cite book}}: Missing or empty|title=(help)CS1 maint: location missing publisher (link)

![{\displaystyle {\begin{aligned}A_{x}&=[{\ce {HA}}]\varepsilon _{{\ce {HA}}}^{x}+[{\ce {A-}}]\varepsilon _{{\ce {A-}}}^{x}\\A_{y}&=[{\ce {HA}}]\varepsilon _{{\ce {HA}}}^{y}+[{\ce {A-}}]\varepsilon _{{\ce {A-}}}^{y}\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/407bba3b954782cbec25c32d99393bf282c2c36d)
![{\displaystyle \mathrm {pH} =\mathrm {p} K_{\mathrm {a} }+\log {\frac {[{\ce {A-}}]}{[{\ce {HA}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2ed476e8f78a1980748a81ec195978b60032411f)




