තැලික් අම්ලය
මෙම ලිපිය වනාහි Phthalic acid ලිපියෙහි ඉංග්රීසි භාෂාවේ සිට සිංහල වෙත නොනිමි පරිවර්තනයකි . ඉංග්රීසි සහ සිංහල යන භාෂාවන්හි සුදුසු හා ප්රමාණවත් පරිචයක් ඇත්නම්, මෙම පරිවර්තනය සම්පූර්ණ කිරීමට ඔබට අවකාශ ඇත. අදාල විෂය පිලිබඳ දැනුවත්නම්, නැවුම් ස්වයං නිර්මාණයක් ලෙස ලිපිය සම්පූර්ණ කිරීමට ඔබට අවකාශ ඇත. |
| |

| |
| Names | |
|---|---|
| වෙනත් නාම
Benzene-1,2-
dicarboxylic acid | |
| Identifiers | |
| CAS number | {{{value}}} |
3D model (JSmol)
|
|
| ChEBI | CHEBI:{{{value}}} |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.001.703 |
| EC Number |
|
| KEGG | {{{value}}} |
| PubChem | {{{value}}} |
| RTECS number | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| SMILES | |
| Properties | |
| Molecular formula | C8H6O4 |
| අණුක ස්කන්ධය | 166.14 g/mol |
| Appearance | white solid |
| Density | 1.593 g/cm3, solid |
| Melting point |
167 °C (sealed tube) |
| Solubility in water | Not soluble |
| Hazards | |
| Related compounds | |
| Related carboxylic acids | Isophthalic acid Terephthalic acid |
| Related compounds | Phthalic anhydride Phthalimide Phthalhydrazide Phthaloyl chloride Benzene-1,2- dicarboxaldehyde |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
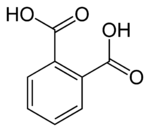
තැලික් අම්ලය (IUPAC systematic name: benzene-1,2-dicarboxylic acid) C6H4(CO2H)2සුත්රය සහිත ඇරෝමැටික ඩයිකාබෝක්සිලික් අම්ලයකි.එය අයිසෝතැලික් අම්ලයේත් ටෙරීතැලික් අම්ලයේත් සමාවයවිකයකි.තැලික් අම්ලය වාණිජමය වටිනාකමින් අඩු වුවත් එහි ව්යුත්පන්නයක් වන තැලික් ඇන්හයිඩ්රයිඩ් (Phthalic anhydride) වාණිජමය රසායන ද්රව්යයක් ලෙස විශාල පරිමාණයෙන් නිපදවයි. [1]
නිෂ්පාදනය
[සංස්කරණය]1836 දී ප්රංශ ජාතික රසායනාඥයෙක් වන ඔගස්ටස් ලුරන්ට් විසින් නැප්තලීන් ටෙට්රාක්ලෝරයිඩ් ඔක්සිකරණයෙන් තැලික් අම්ලය ලබාගන්නා ලදී.ලැබූ ඵලය නැප්තලීන් වල ව්යුත්පන්නයක් යන විශ්වාසය මත ඔහු විසින් නැප්තලෙනික් අම්ලය ලෙස නම් කරන ලදී. ස්විට්සර්ලන්ත ජාතික රසායනාඥයෙක් වූ ජාන් චාර්ල්ස් ගලිසාර්ඩ් ඩි මරිනැක් විසින් නිවැරදි සුත්රය නිශ්චය කර ඊට අදාලව වර්තමානයෙහි පවතින නාමය ලබා දෙන ලදී. නැප්තලීන් උත්ප්රේරක ඔක්සිකරණයෙන් කෙලින්ම තැලික් ඇන්හයිඩ්රයිඩ් බවට හරවා ඇන්හයිඩ්රයිඩය ජලවිච්චේදනයෙන් තැලික් අම්ලය නිෂ්පාදනය කෙරේ.
ප්රතික්රියා හා භාවිතයන්
[සංස්කරණය]
රෝධනය කල නලයකදී (ජලය පිටවීම වලක්වන ලද) ද්රවාංකය 190 °C ක් වූ සුදු පැහැති ස්ඵටිකයකි. භාහිරට විවෘත අවස්ථාවේදී අම්ලය 210 °C දී විලයනය වෙයි.වැඩිපුර හුණු (කැල්සියම් කාබනේට්) සමඟ රත්කළ විට කාබොක්සිල්හරණය හරහා බෙන්සීන් ලබාදෙයි.තැලික් අම්ලයට එස්ටරීකරණය විය හැකි වුවත් එස්ටරීකරණ ප්රතික්රියාව සඳහා භාවිතා වනුයේ වඩා බහුලව පවතින, වඩා ප්රතික්රියාශීලී වූ තැලික් ඇන්හයිඩ්රයිඩයයි.
එය pKa (ආම්ලික විඝටන නියතය) අගයන් 2.89 හා 5.51 වූ ද්වී භාෂ්මික අම්ලයකි.තැලික් අම්ලයේ මොනො පොටෑසියම් ලවනය වන පොටෑසියම් හයිඩ්රජන් තැලේට් විශ්ලේෂනාත්මක රසායන විද්යාවේදී ප්රාමාණික අම්ලයක් ලෙස භාවිතා වෙයි.
තැලික් අම්ලය සෝඩියම් සංරසය සමග ඔක්සිහරණයට ලක් කල විට සයික්ලෝහෙක්සාඩයිඊන් ව්යුත්පන්නයක් ලබා දෙයි.[2]
සමාවයවික
[සංස්කරණය]තැලික් අම්ලය, බෙන්සීන්ඩයිකාබොක්සිලික් අම්ලයේ සංයුතිය සහිත සමාවයවික තුනෙන් එකකි. අනෙක් සමාවයවික දෙක අයිසෝතැලික් අම්ලය හා ටෙරිතැලික් අම්ලය වෙයි. ඇතැම් විට " තැලික් අම්ල " යන යෙදුම මගින් මෙම සමාවයවික කුලය හඳුන්වන මුත් "තැලික් අම්ලය" යන්නෙන් විශේෂයෙන්ම හඳුන්වන්නේ ඔතෝ- සමාවයවිකයයි.
|

|
|
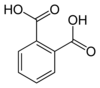
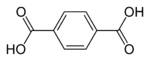
| තැලික් අම්ලය | අයිසොතැලික් අම්ලය | ටෙරීතැලික් අම්ලය |
| (ortho-phthalic acid) | (meta-phthalic acid) | (para-phthalic acid) |
ආරක්ෂාව
[සංස්කරණය]The toxicity of phthalic acid is low with LD50 (mouse) of 550 mg/kg. However, many phthalate esters have been implicated as endocrine disruptors.
මේවාත් බලන්න
[සංස්කරණය]- අයිසොතැලික් අම්ලය
- ටෙරීතැලික් අම්ලය
- තැලේට්
- ටෙරීතැලේට්
- පොටෑසියම් හයිඩ්රජන් තැලේට්, අම්ල-භෂ්ම අනුමාපනයන්හිදී ප්රාථමික ප්රාමාණිකයක්
- තැලික් ඇන්හයිඩ්රයිඩ්
ආශ්රිත
[සංස්කරණය]- ^ Peter M. Lorz, Friedrich K. Towae, Walter Enke, Rudolf Jäckh, Naresh Bhargava, Wolfgang Hillesheim “Phthalic Acid and Derivatives” in Ullmann's Encyclopedia of Industrial Chemistry, 2007, Wiley-VCH, Weinheim.
- ^ සැකිල්ල:OrgSynth
- Merck Index, 9th ed, #7178
භාහිර යොමු
[සංස්කරණය]This article incorporates text from a publication now in the public domain:
Chisholm, Hugh, ed (1911). එන්සයික්ලොපීඩියා බ්රිටැනිකා (11th ed.). Cambridge University Press.
