කාබනික ද්රව්යවල ලක්ෂණ
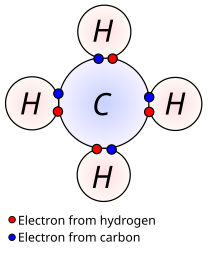
කාබනික සංයෝග සාමාන්යයෙන් සහසංයුජව බැඳී ඇත. දිගු කාබනික දාම සහ වළලු වැනි අද්විතීය ව්යුහයකට මෙය ඉඩ සලසයි. කාබන් අද්වීතිය ව්යුහයක් සැකසීමට දක්ෂ වීමට සහ කාබනික සංයෝග බොහෝ තිබීමට හේතුව වන්නේ කාබනික පරමාණු එකිනෙක සමග ඉතා ස්ථිර සහ සංයුජ බැඳීම් ඇති කරන නිසාය(ධන අයන සෑදීම). අකාබනික මූලද්රව්ය මෙන් නොව කාබනික මූලද්රව්ය සාමාන්යයෙන් දියවීම, වාෂ්ප කිරීම, ගිනිතැබීම හෝ වියෝජනය 3000C ට අඩු උෂ්ණත්වයකදී සිදු කළ හැක. අයන කාබනික සංයෝග පහළ අණුකභාරය සහිත මධ්යසාර සහ හයිඩ්රජන් බන්ධන සිදුවන කාබොක්සිලික් අම්ලය යන විශේෂතා හැරුණු විට අකාබනික ලවණ වලට සමාන කළ විට උදාසීන කාබනික සංයෝග ජලයෙහි අඩුවෙන් දිය වේ.
කාබනික සංයෝග කාබනික රාවකවල පහසුවෙන් දිය වේ. කාබනික ද්රාවක යනු ඊතර් හෝ ඊතයිල් ඇල්කොහොල් වැනි ශුද්ධ සංයෝග හෝ ඛණිජ ඊතර හා සුදු ස්ප්රීතු වැනි ද්රාවණ ආදි වූ මිශ්රණ හෝ භෞතික වියෝජනයේ දී හෝ රසායනික පරිවර්තනවලදී ඛණිජ තෙල්වලින් හෝ තාර කොටස් වලින් ලබා ගනු ලබන නොයෙකුත් ආකාරයේ ශුද්ධ හෝ මිශ්ර සගන්ධ ද්රාවක වේ. නොයෙකුත් ද්රාවකවල ද්රාව්ය ගුණය ද්රාවක වර්ගය සහ ක්රියාකාරී කාණ්ඩ පවත්නේ නම් ඒවා මත බලපැවැත්වේ. ද්රාවණ පිළිබඳ භෞතික රසායන විද්යාව මගින් අධ්යයනය කරනු ලබයි. අකාබනික ලුණු මෙන් කාබනික සංයෝග ද ස්ඵටික සකස් කරයි. කාබනික සංයෝගවල කාබන්වල ඇති විශේෂ ලක්ෂණ වන්නේ වෙනත් මූලද්රව්යවල පරමාණූ මගින් එහි සංයුජතාවය ලබා නොගැනීමයි. එසේ නොකළ විට අසංතෘප්ත තත්වයේ පවතී. මෙවැනි අවස්ථාවලදී අප කාබන් කාබන් ද්විත්ව බන්ධන හෝ ත්රිත්ව බන්ධන පිළිබඳ විමසයි. දාමයක ඒකබන්ධන සමග ද්විත්ව බන්ධන මාරුවෙන් මාරුවට පවතින විට සංයුග්මක ද්විත්ව බන්ධන ලෙස හඳුන්වයි. මෙවැනි සංයුග්මක දාමයක් වැසුණු වළල්ලක් ලෙස පවතින විශේෂ අවස්ථාවකි ඇරෝමැටික ව්යුහය.
