ආසවනය

ආසවනය යනු නටන හෝ පැසෙන ද්රව මිශ්රණයක සංඝටකයන්හී වාෂ්පශීලිතාවයන් ගේ වෙනස්කම් මත පදනම්ව ක්රියාත්මක වන මිශ්රණ වෙන් කිරීමේ ක්රමයකි. ආසවනය, ඒකක ක්රියාවලියක්, හෝ භෞතික විභේදන ක්රියාවලියක් වන අතර, රසායනික ප්රතික්රියාවක් නොවේ.
වාණිජ වශයෙන් ආසවනයේ දී භාවිතයන් කිහිපයක් ඇත. (බොර තෙල් වලින් කොටස් වෙන් කර ගෙන. ප්රවාහනය , බල උත්පාදනය හා තාපනය කිරීම් ආදියට භාවිතා කරයි.) ජලය තුළ වන අපවිත්ර ද්රව්ය ආදිය ඉවත් කිරීමට ජලය ආසවනය කරයි. උදාහරණයක් ලෙස මුහුදු ජලයෙන් ලුණු ඉවත් කිරීම දැක්විය හැක. කාර්මික භාවිතයන් සඳහා ඔක්සිජන් , නයිට්රජන් හා ආගන් වාතය ආසවනයෙන් එකිනෙක වෙන් කොට ගනී. අතීතයේ පැසුණු ද්රාවණ ආසවනය කිරීමෙන් ඇල්කොහොල අන්තර්ගතය අධික ආස්රැත පාන නිෂ්පාදනය කර ඇත.
ආසවනයේ භාවිතයන්[සංස්කරණය]
ආසවනයේ භාවිතයන් රළු වශයෙන් ප්රධාන කොටස් 4කට බෙදා දැක්විය හැක. ඒවා නම් පරීක්ෂණාගාර මිනුමක් ලෙස , කාර්මික ආසවනය , බෙහෙත් ආසවනය මගින් සුවඳ විලවුන්වලට හා ඖෂධවලට හා ආහාර සැකසුමේ දී වේ. පසුව සදහන් කළ දෙක පෙර සඳහන් කළ භාවිතයන් දෙක මෙන් පවිත්රකරණයට ලක් නොකරන ක්රමවේදයක් වන අතර සියළු වාෂ්පශීලී ආස්රැතයට මුල් ද්රාවණයෙන් ලබා ගනී.
පරීක්ෂණාගාර පරිමාණයේ හා කාර්මික පරිමාණයේ ආසවනයන්හි ප්රධානතම වෙනස නම් පරීක්ෂණාගාර ආසවනය කාණ්ඩ වශයෙන් සිදු කරයි. නමුත් කාර්මික ආසවනය නොනැවතී සිදු කරයි. කාණ්ඩ ආසවනයේ දී ආසවන ප්රභවය ආසවනය වූ සංයෝග හා ආස්රැතය අසාවන ක්රියාවලියේදී නිරතුරුව වෙනස් වේ. කාණ්ඩ ආසවනයේදී ආසවකය පිරුණු මිශ්රණයක් විශාල ප්රමාණවලින් එවීමට සළස්වයි. පසුව එය කුඩා කොටස්වලට කැඩුණු පසු වාෂ්පශීලීම සංයෝගයේ සිට අඩු වාෂ්පශීලීතාවයෙන් යුත් සංයෝගය වෙන් කර ගනී. (ඉතිරිවන සංයෝගය වාෂ්පශීලීතාව අවම හෝ වාෂ්පශීලී නොවන සංයෝගයකි) පතුලේ ඉතිරි වන වාෂ්පශීලීතාවයෙන් අඩුම සංයෝගය අවසානයේ දී එකතු කර ගනී. අසාවකය නැවත වෙනස් කරමින් ක්රියාවලිය නැවත ක්රියාත්මක වේ.
සන්තතික ආසවන ක්රියාවලියේ දී ආරම්භක ප්රභව , වාෂ්පය හා ආස්රැතය නියත සංයුතියක පවත්වා ගනී. මේ සදහා පරිස්සමෙන් ආරම්භක පරිස්සමින් ආරම්භක ප්රභවය නැවත පුරවමින් කැඩුණු සංයෝග වන වාෂ්පය හා ද්රවය පද්ධතියෙන් ඉවත් කරයි. මෙය සාර්ථක විභේදනය කිරීමේ ක්රියාවලියක් පාලනය කිරීමට හේතු වේ.
අනෙක් අවස්ථාවල රවුල්ගේ හා වොල්ටන්ගේ නියමවලින් අපගමන දක්වයි. ප්රසිද්ධතම අපගමන පෙන්වනු ලබන්නේ එතනෝල් හා ජලය මිශ්රණයයි. මෙම මිශ්රණය එක්ව ගෙන රත් කළ විට ඇසයොට්රෝපයක් නිර්මාණය වන අතර එම මිශ්රණයේ තාපාංකය සංරචක දෙකෙහිම තාපාංකවලට වඩා අඩු අගයක් පෙන්වයි. සැබැවින්ම සියළු ද්රවණ මිශ්ර කර රත් කළ විට ඇසයෝට්රෝෆික හැසිරීමක් පෙන්වයි. මෙසේ හැසිරීම් පෙන්වන සංයෝග සඳහා සංඛ්යාත්මක ගණය කිරීමේ ක්රම තිබුණ ද මේවායේ හැසිරීම් අනුමාන කිරීමට ඇති එකම ක්රමය වන්නේ වාෂ්ප - ද්රව සමතුලිත දත්ත පමණි.
ආසවනයෙන් පමණක් මිශ්රණයක් පිරිසිදු කිරීම සිදු නොවන්නකි. මෙය වීමට සංරචක මිශ්රණය තුළ ශූන්ය ආංශික පීඩනයක් පැවතිය යුතුවේ. අති සංශුද්ධ - ද්රව්ය ලබා ගැනීමට අරමුණු වේ. මේ වෙනත් රසායනික වෙන් කිරීමේ ක්රියාවලි අනුගමනය කළ යුතු වේ.
ඛාණ්ඩ ආසවනය[සංස්කරණය]
ඛාණ්ඩ ආසවකය A හා B වෙන් කිරීමේ ක්රියාවලිය පෙන්වයි.
පරිපූර්ණ වාෂ්පශීලී A හා B (A හි වාෂ්පශීලීතාවය වැඩිය තාපාංකය අඩු අගයකි) සංයෝග මිශ්රණය එම මිශ්රණය එහි වාෂ්පය එන තෙක් ඛාණ්ඩ ආසවනය රත් කරයි. (මුල් කොටස්වල මෙය වචනයෙන් විස්තර කොට ඇත) වාෂ්පයේ A හා B අතර අනුපාතය ද්රවයේ A හා B අතර අනුපාතයෙන් වෙනස් විය හැක. ද්රව මිශ්රණයේ A හා B අතර අනුපාතය එය පිළියෙල කළ අයුරු මත රදා පවතී. වඩාත් වාෂ්පය සංයෝගයෙන් වාෂ්පය සාරවත් වේ. (රවුල්ගේ නියමයට අනුව) කන්ඩෙන්සරය තුළින් වාෂ්පය යමින් පද්ධතියෙන් ඉවත් වේ. මෙයින් පෙනී යන්නේ ඉතිරි වන ද්රාවණයේ සංයුතියෙන් වෙනස් වන බවයි. (B ගෙන් වඩාත් සාර වේ)
ප්රතිඵලය වනුයේ ද්රාවණය තුළ ද්රාවණ මිශ්රණයේ අනුපාතය වෙනස් වී වඩාත් B ගෙන් ද්රාවණය සාරවත් වීමයි. මෙය ද්රව මිශ්රණයේ තාපාංකය ඉහළ යැවීමට හේතු වේ. වාෂ්ප මිශ්රණයේ උෂ්ණත්වය ඉහළ නැංවීමට ද හේතු වේ.
පරිසමාප්ත ආසවන ආකෘතිය[සංස්කරණය]
ද්රවයක් නටනු ලබන්නේ ද්රවයේ වාෂ්ප පීඩනය අවට පරිසරයේ පීඩනයට සමාන වන උෂ්ණත්වයේදීය. සාමාන්ය තාපාංකය යනු විශේෂ අවස්ථාවක් එනම් වාෂ්ප පීඩනය හා අවට වායුගෝලීය පීඩන සමාන වූ අවස්ථාවයි. බදුනක් තුළ ද්රවයක පීඩනය වායුගෝලීය පීඩනයට වඩා අඩු නම් එය සාමාන්ය තාපාංකයට වඩා අඩු උෂ්ණත්වයකදී නටන අතර බදුනක් තුළ ඇති ද්රවයක පීඩනය වායුගෝලීය පීඩනයට වඩා වැඩි නම් සාමාන්ය තාපාංකයට වඩා වැඩි උෂ්ණත්වයකදී නටයි. ද්රාවණ මිශ්රණයක් ගෙන එයට දුන් පීඩනයක් යටතේ නැටවූ විට අදාල සංයෝගය පමණක් තාපාංකයේදී දුන් පීඩනයට අනුව වාෂ්ප වූ විට එකතු කිරීමේ ක්රමයක් පොදු වැරදි වැටහීමක් තිබුණි. නමුත් මෙය පරිසමාප්ත පද්ධතියක පවා සිදු නොවන්නකි. පරිසමාප්ත ආසවන අකෘතිය පාලනය වන්නේ රවුල්ගේ නියමය හා ඩොල්ටන්ගේ නියමයයි.
රවුල්ගේ නියමයෙන් පෙන්වනු ලබන්නේ සංරචකයක් මුළු වාෂ්ප පීඩනයට දක්වන දායකත්වය එහි ප්රතිශතයක් ලෙස ගත් විට එය සංශුද්ධව ඇති විට දක්වන පීඩනය වේ. සංරචකයක් තවත් සංරචකය වාෂ්ප පීඩනයම වූවොත් හෝ සංරචකයක වාෂ්පශීලීතාව මිශ්රණය තුළ එහි ප්රතිශතය මත රදා පැවතුණහොත් නියමයට එකග නොවේ.
ඩෝල්ටන්ගේ නියමයෙන් පෙන්වනු ලබන්නේ මුළු වාෂ්ප පීඩනය සංරචක එක එකක් ලෙස ගත් කළ දක්වන වාෂ්ප පීඩනයන්ගේ ඓක්යය බවයි. බහු සංරචක ද්රාවණයක් රත් කළ විට එක් එක් සංරචකයන්ගේ වාෂ්ප පීඩනයන් ඉහළ යයි. මෙලෙස මුළු වාෂ්ප පීඩනය ඉහළ යයි. මෙලෙස පීඩනය වැඩිවී අවට වායුගෝලයේ පීඩනය දක්වා ළගා වූ විට මිශ්රණය නැටීමට පටන් ගනී. ද්රාවණය නැටීමට පටන් ගැනීමෙන් පසු ද්රාවණයෙන් විශාල වශයෙන් වාෂ්පය නිකුත් වීමට පටන් ගනී. අන්යෝන්ය වශයෙන් ද්රාව්ය මිශ්රණයකට දුන් පීඩනයකට ඇත්තේ එක් තාපාංකයක් බව සදහන් කරගන්න.
පරිසමාප්ත ආකෘතිය රසායනික වශයෙන් ද්රව්යයන් සම්බන්ධයෙන් නිවැරදි වේ. ඒවා නම් බෙන්සීන් හා ටොලුයීන් වැනි ඒවාය. මෙමගින් වාෂ්පය තුළ A:B සංයුතිය වෙනස් වීමට ද හේතුවේ. (ආසවනය ක්රියාත්මකවත්ම B හි වායුමය කලාපයේ වැඩිවීමක් දක්නට ඇත. මෙය ආස්රැතයේ A:B අනුපාතය වෙනස්වත්ම පවතින වෙනස විශාල නම් (සාමාන්යයෙන් තාපාංකවල වෙනස සලකා බලයි.) ආරම්භක මිශ්රණය A ගෙන් සාරවත් අතර ආසවනය කළ පසු A ආසවනය වී අවසන් වන අතර නටන ද්රාවණය B සංරචකයෙන් සාරවත් වේ.
සන්තතික ආසවනය[සංස්කරණය]
සන්තතික ආසවනය යනු ආසවන මිශ්රණයක් නොකඩවා සපයමින් වෙන්වන සංරචක පිටාර ප්රවාහ ලෙස ඉවත් කරමින් ඉදිරියට යන ක්රියාවලියකි. සන්තතික ආසවනයක් අඩුම වශයෙන් ප්රතිදාන දෙකක් වන් නිෂ්පාදනය කරයි. වාෂ්පශීලී ආස්රැත සංරචකය , තාපාංකයේදී වාෂ්ප වූ වාෂ්පය එකතු කරගෙන ද්රවය දක්වා සාන්ද්ර කොටගත් ද්රවයෙන් අන්තර්ගතය. සෑම විටම පතුලේ සංරචකයක් (ඉතිරිව) තිබෙන අතර එය වාෂ්පශීලිතාවයෙන් අඩුවන අතර සාන්ද්ර කළ වාෂ්පයක් ලෙස එය එකතු කර නොගනී.
පොදුවේ ලබා ඇති දියුණු වීම්[සංස්කරණය]
ඛාණ්ඩ සන්තතික යන ආසවන ක්රියාවලි 2 හිම ආසවන ප්ලාස්කුවට ඉහළින් විභාජක කුළුණක් සවි කිරීමෙන් කාර්යක්ෂමතාවය වැඩි කළ හැක. විභාජක කුළුණ මගින් වාෂ්පය විශාල ප්රදේශයක ගැටෙමින් ඝනීභූත වීමට හැකියාව ලැබීමෙන් විභේදන ක්රියාවලිය දියුණු වේ. සමතුලිතතාවයට එළඹීමට ගතවන කාලය වැඩි කිරීම මගින් ද උදව් සැලසේ. විභාජක කුළුන ද්විතීක පද්ධතිවලින් ද සමන්විත විය හැක. (බදුන් හෝ තැටි) ඒවායින් නටන ද්රව මිශ්රණවලින් සාරවත්ව ඒවායේ වාෂ්ප - ද්රව සමතුලිතතාවයන් පැවතීම උපකාරී වේ.
පරීෂණාගාර හා කාර්මික පරිමාණයේ විභාජක කුළුන යම් යම් වෙනස්කම් දක්නට ලැබුණ ද ඒවායේ භාවිතා වනුයේ එකම මූලධර්මයයි. උදාහරණ වශයෙන් කාර්මික පරිමාණයේ විභාජක කුළුන (සඵලත්වය වැඩීමට)
- වායු කන්ඩෙන්සරයක්
- විභාජක කුළුණ (සාමාන්යයෙන් පරීක්ෂණාගාර පරිමාණයේ පමණි)
- ඇහුරූ කුළුණ (වීදුරු පබළු , ලෝහ කැබලි හෝ අනෙක් රසායනිකව නිෂ්ක්රීය සංයෝගවලින් අසුරා ඇත)
- භ්රමණ ආසවන කලාප පද්ධතිය
පරීක්ෂණාගාර පරිමාණයේ ආසවනය[සංස්කරණය]
පරීක්ෂණාගාර පරිමාණයේ ආසවනයේදී මුළුමනින්ම පාහේ ඛාණ්ඩ ආසවන සිදු කෙරේ. ආසවනයේ දී යොදාගන්නා උපකරණය ආසවකය ලෙස හඳුන්වයි. එය අවම වශයෙන් ප්රතිබොයිලේරුවකින් හෝ ප්රභවය ඇති බඳුන තාපනය කිරීම් ක්රමවේදයකින් , රත් වූ වාෂ්පය ද්රව අවස්ථාවට සිසිල් කරන කන්ඩෙන්සරයකින් සහ ඝනීභවනය කරන ලද පිරිසිදු කළ ද්රවය එනම් ආස්රැතය ලබා ගැනීම් ක්රමවේදයකින් සමන්විත විය යුතුය. ආසවනය සඳහා පරීක්ෂණාගාර පරිමාණයේ තාක්ෂණික ක්රමවේද පවතී.
සාමාන්ය ආසවනය[සංස්කරණය]
සාමාන්ය ආසවනයේ දී සියළුම උණුසුම් වාෂ්පය කන්ඩෙන්සරයක් වෙත යොමු කර සිසිල් කර ඝනීභූත කර ගනී. එහෙයින් ආස්රැතය පිරිසිදු නොවන අතර එහි සංයුතිය එම උෂ්ණත්වය පීඩනයේ එහි අන්තර්ගත වාෂ්පවල සංයුති වන අතර ඒවා රවුල් නියමයෙන් ගණනය කළ හැකි වේ.
සාමාන්යයෙන් ‘සාමාන්ය ආසවනය’ තාපාංක අතර විශාල වෙනසක් (ආනුභූතිය රීතිය වන්නේ 250C කි) ඇති ද්රව එකිනෙක ගෙන වෙන් කිරීමට හෝ පහසුවෙන් වාෂ්ප නොවන ද්රාවණ හෝ තෙල්වලින් ද්රාවණ වෙන් කිරීමට භාවිතා කරයි. මෙවැනි කාරණා සඳහා සංයෝගවල වාෂ්ප පීඩන සාමාන්යයෙන් ප්රමාණවත් වන අතර රවුල්ගේ නියමයේ එන වෙනස්කම් නොසලකමින් කටයුතු කරයි. මන්ද යත් වාෂ්පශීලීතාවයෙන් අඩු සංයෝගය ප්රමාණවත් දායකත්වයක් දරණ බැවිනි.
භාගික ආසවනය[සංස්කරණය]
බොහෝ අවස්ථාවලදී මිශ්රණය තුළ වන බොහෝ සංයෝගවල තාපාංක ප්රමාණවත් තරම් ළගින් පිහිටන බැවින් රවුල්ගේ නියමය සැළකිල්ලට භාජනය කළයුතු වේ. භාගික ආසවනයේදී සංයෝග වෙන් කිරීමට වාෂ්පීකරණය - ඝනීභවනය යන ක්රියාවලි නැවත නැවත හොඳින් විභාජක කුළුනක සිදුකළ යුතුය.
පිරිසිදු කිරීමට අවශ්ය ද්රාවණය රත් කරයි. එවිට එහි වාෂ්පය විභාජක කුළුන දිගේ ඉහළට නගී. එය කුළුන දිගේ ඉහළට නැගිත්ම ඝනීකාරක බිත්ති දිගේ හා ඇහුරූ ද්රව්ය ඇති ප්රදේශවලට ගොස් සිසිල් ඝනීභවනය වේ. මෙහිදී සංඝනීභූතය ඉහළ යන උණුසුම් වාෂ්පය මගින් යලිත් තාපවත් වේ. එමගින් එය යලිත් වාෂ්පීකරණය වේ. කෙසේ වෙතත් රවුල්ගේ නියමයෙන් නැවුම් වාෂ්පයේ සංයුතිය නැවත තීරණය කරනු ලැබේ. එක් එක් වාෂ්පීකරණ - ඝනීභවන චක්රයක් පාසාම (සෛද්ධාන්තික තැටි) වඩාත් වාෂ්පශීලී සංයෝගයෙන් යුත් ඵලදාවක් ලබාදේ. සත්ය වශයෙන් දී ඇති උෂ්ණත්වයකි. එක් එක් චක්රයකදී හරියටම විභාජක කුළුණේ දී ඇති ස්ථානයක සිදු නොවේ. සෛද්ධාන්තික තැටි නිවැරදි පැහැදිලි කිරීමට වඩා සුදුසු සංකල්පයකි.
හුමාල ආසවනය[සංස්කරණය]
රික්තීය ආසවනය මෙන් හුමාල ආසවනය යනු තාප සංවේදී සංයෝග ආසවනය කිරීමේ ක්රමවේදයකි. තාපනය කළ අමුද්රව්ය මිශ්රණය තුළින් බුබුලන හුමාලයක් යැවීම ක්රියාවලියකි. රවුල්ගේ නියමයට ඉලක්ක කරගත් සමහර සංයෝග වාෂ්පීභවනය වේ. (එහි ආංශික පීඩනයට අනුව) වාෂ්පය සිසිල් කර ඝනීභවනය කරනු ලැබේ. සාමාන්යයෙන් තෙල් සහ ජලීය ස්තරයකින් සමන්විත වේ.
හුමාල ආසවනය මගින් සුගන්ධ ඖෂධ සහ මල් භාවිතයෙයන් නිෂ්පාදන 2ක් කරයි. සුගන්ධ තෙල් මෙන්ම ජලීය ඖෂධීය ආස්රැත මෙම සුගන්ධ තෙල් සුවද ද්රව්ය නිපදවන තැන්වල සහ ඇරෝමාතෙරපි ආහාර සකස් කිරීමේදී හා සමට සාත්තු කිරීමට භාවිතා කරයි.

ඩයිමෙතිල් සල්ෆොක්සයිඩ් සාමාන්යයෙන් 1890C නටයි. රික්තයක් තුළ එය ආසවනය වී ග්රාහකයට 700C දී වැටෙයි.

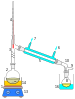
1. මන්ත දණ්ඩ / ගැස්සෙමින් නටන කුඩා ඇට : 2. ආසවක බදුන : 3. විභාජක කුළුන : 4. උෂ්ණත්වමානය / තාපාංකය තෙක් උෂ්ණත්වය මිනිය හැකි : 5. ටෙෆ්ලෝන් කරාම : 6. සිසිල් ඇගිල්ලක් වැනි දැයක් : 7. සිසිල් ජලය ඇතුළු වීම : 8. සිසිල් ජලය පිටවීම : 9. ටෙෆ්ලෝන් කරාමය : 10. වාෂ්පය හෝ වායුවේ ඇතුළු වීම. : 11. ටෙෆ්ලෝන් කරාමය
රික්ත ආසවනය[සංස්කරණය]
සමහරක් සංයෝග සතුව ඉහළ තාපාංක පවතී. එවැනි සංයෝග නැටවීමට උෂ්ණත්වය වැඩි කිරීම පසෙකලා පීඩනය අඩු කිරීම වඩා යෝග්ය වේ. සංයෝගයේ වාෂ්ප පීඩනයට වඩා වරක් පීඩනය අඩු කළ විට (අදාල උෂ්ණත්වයේදී ) නැටීම සහ ආසවනයේ අනෙක් ක්රියාවලීන් ආරම්භ කළ හැකිය. මෙම තාක්ෂණය රික්ත ආසවනය ලෙස හඳුන්වන අතර පරීෂණාගාරයක් සුළභව දක්නට ලැබෙන බමන වාෂ්පීකරණය තුළ මෙය දක්නට ඇත.
මෙම තාක්ෂණය මගින් සංයෝගයක් වියෝජනය උෂ්ණත්වය ඉක්මවා වායුගෝලීය පීඩනය තුළ නැටවීමට ඉතා ප්රයෝජනවත් සහ වායුගෝලීය පීඩනයට අඩු පීඩනයේදී වියෝජනය කර නැටවීමට උත්සාහ කිරීමට ප්රයෝජනවත්ය.
වායු සංවේදී ආසවනය[සංස්කරණය]
සමහරක් සංයෝග සංවේදීව තිබී ඒවාට උච්ච තාපාංක පිහිටයි. සාමාන්ය රික්ත ආසවන පද්ධතියක් උදාහරණයක් ලෙස ඉහත අවස්ථාවට භාවිතා කළ හැක. ඒ මගින් රික්තය නිෂ්ක්රීය වායුවක් ආසවනයෙන් පසු ඇතුළු කිරීම සිදු කරයි. කෙසේ වෙතත් මෙය තෘප්තිමත් විය නොහැකි පද්ධතියකි. යමෙක් අඩු පීඩනයක් යටතේ කැඩුණු කොටස් එකතු කිරීමට සිතන්නේ නම් විග් ඇඩැප්ටරයක් කැන්ඩෙන්සරයේ අගට සවි කළ යුතු වේ. වඩාත් හොද ප්රතිඵල හෝ සංවේදී සංයෝග සදහා පර්කින් ට්රයිඇන්ගල් උපකරණ භාවිතා කළ හැක.
පර්කින් ට්රයිඇන්ගල් සතුව විවිධ උපක්රම පවතී. කැඩුණු සංයෝග ආසවකයෙන් වෙන් කිරීමට ටෙෆ්ලෝන් කරාම උපකාරී වේ. ඒ සඳහා ප්රධාන ආසවන කළ හෝ වාෂ්පය හෝ තාපන මූලාවයවය වෙන් කිරීම අත්යාවශ්ය නොවේ. එය ප්රතිභාව වාෂ්පයෙන් වෙන්කර ගැනීමට කරාම භාවිතා කළ හැක. සාම්පලය තුළ වාෂ්පය නිෂ්ක්රීය වායුවක් (නයිට්රජන් හෝ ආගන්) මගින් ප්රතිස්ථාපනය ඉවත් කළ හැක. නැවුම් සමුච්චයක් සහිත බඳුන දැන් පද්ධතියට සවි කළ හැක. ආසවන පද්ධතිය අත්හැර එය සවිකර කරාම මගින් දෙවනුව කැඩුණු කොටස් ගත හැක. මෙලෙස මෙය දිගට අවසානය තෙක් ......... සියළු කැඩුණු කොටස් එකතු කර ගන්නා තෙක් සිදු කළ හැක.
ලුහු මං ආසවනය[සංස්කරණය]
ලුහු මං ආසවනය උපකරණ කට්ටලයේ සිරස්ව පිහිටි කන්ඩෙන්සරයක් සමන්විත වීමක් ආසවන මාර්ගය කෙටී වී ඇත.
1.මන්ත දණ්ඩක් සහිත ආසවක බදුන / ගැස්සෙමින් නටන කුඩා ඇට. : 2. සිසිල් ඇගිල්ලක් වැනි දෙයක් - කෙළින්ම ඝනීභූත කිරීමේ අභිප්රායට : 3. සිසිල් ජලය ඇතළු වීම : 5. වාෂ්පය / වායුව ඇතුළු වීම : 6. ආස්රැත ප්ලාස්කුව / ආස්රැතය
ලුහුමං ආසවනය යනු ආස්රැතය කෙටි දුරක් එනම් සෙන්ටිමීටර කිහිපයක් ගමන් කරවීමේ ආසවන තාක්ෂණ උපක්රමයකි. සාම්ප්රදායික උදාහරණය වනුයේ ආස්රැතය වීදුරු බල්බයෙන් බල්බයට ආසවනයේදී ගමන් කරයි. නමුත් කන්ඩෙන්සරයේ කුටීර දෙකක අවශ්යතාවයක් පැන නොගනී. මෙම තාක්ෂණය අධික උෂ්ණත්වලදී අස්ථායී සංයෝග සඳහා බහුලව භාවිතා කෙරේ. මෙහි ඇති වාසිය වනුයේ තාපනය කළ යුතු උෂ්ණත්වය සැළකිය යුතු ලෙස පහත් අගයක් වන අතර (මෙම අඩු කළ පීඩනය හේතුවෙන්) සහ ආස්රැතයට ඝනීභවනය වීමට පෙර ගමන් කිරීමට ඇත්තේ අඩු දිගක් වීමයි. කියුග් ලෝහ උපකරණ කට්ටලය කෙටි මං ආසවයට භාවිතා කළ හැක.
වෙනත් ආකාර[සංස්කරණය]
- භ්රමණ වාෂ්පීකරණයේදී රික්ත ආසවන උපකරණ කට්ටලය සාම්පයක මහත් ලෙස දියවූ ද්රව්ය ඉවත් කිරීමට යොදා ගනී. රික්තය සාදා ගනු ලබන්නේ ජල චූෂකයක් හෝ පටල පොම්පයක් මගිනි.
- කියුග්ලෝහ එනම් කෙටි මං ආසවන උපකරණය (සාමාන්යයෙන් ඉහළ රික්තයකින් සමන්විත වේ) සාමාන්යයෙන් ඉහළ තාපාංක (> 3000C ) සහිත සංයෝග ආසවනය කිරීමට භාවිතා කරයි. මෙම උපකරණය උදුනකින් සමන්විතය. ආසවනය වූ සංයෝගය එහි තැබීමට ඉඩ ඇත. ප්රතිදාන අංශය උදුනෙන් බාහිරව පිහිටා ඇත. සාම්පලය බමනය කිරීම් උපක්රමද අන්තර්ගතය. ප්රබල රික්ත පොම්පයක් මගින් රික්තය තනා ගනී.
- ප්රතික්රියාවක් පෙන්වන ආසවනයේදී ප්රතික්රියා බදුන ආසවකය ලෙස භාවිතා කරයි. මෙම ක්රියාවලියේදී ප්රතික්රියකවලට වඩා සැළකිය යුතු තරම් අඩු තාපාංකයක් ඇත. ප්රතිඵල සෑදීමත් සමග ප්රතික්රියක වාෂ්ප වී ප්රතික්රියා මිශ්රණයෙන් ඉවත්ව යයි. මෙම තාක්ෂණය නොනැවතුණු සරල කම්පනයට උදාහරණයකි. සමූහ ක්රියාවලියේ දී වාසිතම ප්රතික්රියා බදුන පිරවීමට අඩු කාලයක් සහ පහසුවෙන් කළ හැකි වීම.
- සංහාරක ආසවනයට ඝන ද්රව්ය ප්රබල ලෙස තාපනය කිරීම් (නිරතුරුව කාබනික පදාර්ථ) ඔක්සිජන් (දහනයෙන් වළක්වා) නොමැතිව ඉහළ තාපාංක සහිත ද්රව වාෂ්ප කිරීමට මෙන්ම තාප අස්ථායී සංයෝග සඳහා සහභාගී වේ. ලී සංහාරක ආසවනයේ භාවිතයෙන් මෙතනෝල් ලබා ගනී. එහි දන්නා නම වනුයේ ‘වුඩ් ඇල්කොහොල්’ය.
- පූර්ව වාෂ්පීකරණය . විවර පටලයක් මගින් ආංශිකව වාෂ්ප කිරීමත් හරහා මිශ්රණවලින් වෙන් කිරීමේ ක්රමවේදයකි.
- වියලි ආසවනය ඇත්ත වශයෙන් නමෙන් දැක්වෙන පරිදි එය ආසවනයක් නොවේ. තාප විච්ඡේදන ප්රතික්රියාවක් ඔස්සේ ඝන ද්රව්ය ප්රබල ලෙස ඔක්සිහරණය කර වාෂ්පශීලි සංරචක වෙන්කර ගනී.
- නිස්සාරක ආසවනය. ආසවනය ඉදිරියේ මිශ්ර කළ හැකි ඉහළ තාපාංක ඇති සාපේක්ෂව වාෂ්පශීලී නොවන හොදින් දියවන මිශ්රණයේ අනෙක් ද්රව්ය සමග ඇසයොට්රෝප නොසාදන ලෙස අර්ථ දක්වා ඇත.
- ක්ෂණික වාෂ්පීකරණය (හෝ ආංශික වාෂ්පීකරණය ) යනු ආංශික වාෂ්පීකරණය අවකරණ උපාංගයක් හෝ අවකරණ කපාටයක් තුළින් වාෂ්ප පීඩනය අඩු කර ගනීමෙන් සංතෘප්ත කර ගනී. මෙම ක්රියාවලියේ සරලතම අංගයකි. සිසිල් ආසවනය යනු හිමායනය මගින් පවිත්රකරණය කිරීමේ ක්රමවේදයකි. මෙය වාෂ්පීකරණය වෙනුවට කරන්නකි. මෙය ඇත්තෙන්ම ආසවනය නොවේ එසේම ආසවනයේ මෙන් සමාන ඵල මෙහිදී නොසෑදේ. මෙම ක්රියාවලිය පිළිවෙලින් අයිස් බියර් හා අයිස් වයින්හි එතනෝල් හා සීනි අන්තර්ගත වැඩි බිම භාවිතා කරයි.
- සමාසවනය යනු මිශ්ර කිරීමේ හැකියාවක් නොමැති සංයෝග මිශ්රණයක් ආසවනය කිරීමයි.
සාමාන්ය කාර්මික ආසවන කුළුණු[සංස්කරණය]

මහාපරිමාණ කාර්මික ආසවනය කාණ්ඩ වශයෙන් හෝ සන්තතව සිදු කරන නිෂ්පාදන ක්රියාවලීන්හිදි භාවිත කෙරෙන අතර එහිදි භාගික ආසවනය, රික්තක ආසවනය, වාෂ්ප ආසවනය, නිස්සාරක ආසවනය සහ ඇසෙයෝට්රෝපික ආසවනය ආදි ක්රම වේද භාවිත වේ. සන්තතික අචල තත්ත්ව භාගික ආසවනය වඩාත් බහුලව භාවිත වන්නේ ඛණිජ තෙල් පිරිපහදුව ඛනිජ රසායනික සහ රසායනික කර්මාන්ත ශාලා සහ ස්වභාවික වායු සැකසුම් කර්මාන්ත ශාලා ආදිය තුළ වේ.
කාර්මික ආසවනය සඳහා ආසවන කුළුණු ලෙස හැඳින්වෙන විශාල සිරස් සිලිණ්ඩරාකාර කුළුණු භාවිතා වන අතර ඒවායේ විෂ්කම්භය සෙ.මි. 65 සිට මිටර් 16 ක් දක්වා විය හැකි අතර උස ප්රමාණය මීටර් 6 සිට 90 දක්වා වේ. ඇතැම් විට මිටර් 90 වටද වඩා උසින් වැඩි කුළුණු භාවිතා විය හැකිය. සැකසුම සඳහා කුළුණු තුළට ඇතුල් කෙරෙන ද්රවය ද්රව කිහිපයක මිශ්රණයකින් තැනි ඇති විට කුළුණුවල විවිධ උස ප්රමාණ වලින් පිහිටා ඇති පිටවුම් මං ඔස්සේ එකිනෙකට වෙනස් තාපාංක හා තාපාංක පරාස ඇති විවිධ භාගයන් නැතහොත් විවිධ නිෂ්පාදන වෙන්කර ගත හැකිය. මේ අතරින් වඩාත් සැහැල්ලුතම නිෂ්පාදන (අඩුම තාපාංක සහිත නිෂ්පාදන) කුළුණුවල ඉහළින්ම ලබාගෙන යන අතර වඩාත් බරින් වැඩි නිෂ්පාදන (වැඩිම තාපාංක සහිත නිෂ්පාදන) කුළුණුවල පහළම කෙළවරින් වෙන්කර ගැනේ.
විශාල පරිමාණ ආසවන කුළුණුවලදී වඩාත් පුර්ණ ආකාරයෙන් නිෂ්පාදන වෙන්කර ගැනීම සඳහා ප්රතිවාහ ක්රමය භාවිත කෙරේ. ප්රතිවාහ ක්රමයේදී ඉහත සාමාන්ය මහාපරිමාණ කාර්මික ආසවන කුළුණක දැක්වෙන පරිදි ආසවන හෝ විභාජක කුළුණකින් ලබාගත් ද්රවිත ඵලයන්වලින් කොටසක් නැවත එම කුළුණෙහිම ඉහළ කෙළවරින් ඇතුල් කෙරේ. කුළුණ තුලදී පහළට ගමන් කරන ප්රතිවාහ ද්රවය මගින් ඉහළට පැමිණෙන වාෂ්පය සිසිල් කිරීම සහ ඝනීභවනය කිරීම සිදු කෙරෙන අතර ඒ ඔස්සේ ආසවන කුළුණේ කාර්යක්ෂමතාව ඉහළයයි. සෛද්ධාන්තිකව දෙන ලද විභාජක මට්ටම් ප්රමාණයක් සහිත ආසවන කුළුණකට මෙසේ ඇතුළු කළ හැකි ප්රතිවාහ ප්රමාණය වැඩිවන විට කුළුණ මගින් ඉහළ තාපාංක ඇති ද්රව්ය පහළ තාපාංක ඇති ද්රව්ය වලින් වෙන්කිරීමේ ක්රියාවලිය වඩාත් හොදින් සිදුවේ. කිසියම් නිශ්චිත විභාජනයක් සඳහා භාවිත කළ හැකි ප්රතිවාහ ප්රමාණය වැඩිවන විට ඒ සඳහා භාවිත කළ යුතු විභාජන මට්ටම් සංඛ්යාව පහළ යයි.
මේ ආකාර කාර්මික ආසවන කුළුණු වාතයෙන් ද්රවිත ඔක්සිජන්, ද්රවිත නයිට්රජන් සහ අතිශය සංශුද්ධ ආගන් වායු වෙන්කර ගැනීමේදී භාවිත කෙරේ. අර්ධ සන්නායක නිෂ්පාදනය සඳහා යොදා ගන්නා අතිශය සංශුද්ධ සිලිකන් නිපදවීම සදහා ක්ලෝරෝසිලෙන් ආසවනය යොදා ගත හැකිය.
කාර්මික ආසවන කුළුණක හරස්කඩ - මෙහි කුලුණේ විවිධ මට්ටම් සහ ඒවායේ ඇති බුබුලුවහන්තරා දැක්වේ.
ආසවන කුළුණු නිර්මාණය සහ ඒවා ක්රියාවේ යෙදවීම ආසවනය කළ යුතු ද්රව්ය සහ ඉන් ලබාගත යුතු නිෂ්පාදන මත රදාපවතී. ආසවනය කළ යුත්තේ සරල සංරචක යුගලකින් යුත් ද්රව්යයක් වේ නම් මැක්කේබ්-තීලේ ක්රමය හෝ ෆෙන්ස්කේ සමීකරණය වැනි විශ්ලේෂණ ක්රමයක් භාවිත කළ හැකිය. නමුත් ආසවනය කළ යුතු අමුද්රව්ය ද්රව්ය විශාල සංඛ්යාවකින් සමන්විත වේ නම් කුළුණු නිර්මාණය සහ භාවිතයේදී සමාකරණ ආදර්ශන ක්රමවේද භාවිත කළ යුතු වේ. තවද ආසවන කුළුණුවලදී භාවිතා වන වාෂ්ප - ද්රව ස්පර්ශක උපාංග (මට්ටම්) වල කාර්යක්ෂමතාව, සෛද්ධාන්තිකව ලැබෙන 100% සමතුලිත තත්ත්වයට වඩා අඩුවේ. එබැවින් ආසවන කුළුණක් සඳහා සෛද්ධාන්තිකව ලැබෙන වාෂ්ප - ද්රව සමතුලිතතා අවස්ථා ගණනට වඩා වැඩි මට්ටම් සංඛ්යාවක් පැවතිය යුතුය.
කාර්මික යෙදුම් වලදී ඇතැම් විට කුළුණ තුල - මට්ටම් වෙනුවට ඇසුරුම් ද්රව්යයක් භාවිත කෙරේ. රික්තක තත්ව යටතේ ක්රියාත්මක වන අවස්ථා වැනි කුළුණ හරහා අඩු පීඩන පාතනයක් අවශ්ය වන අවස්ථා වලදී මෙය විශේෂයෙන් භාවිත වේ.
මෙම ඇසුරුම් ද්රව්ය විශේෂ ඇසුරුම් ක්රමයකින් තොරව ඇතුල්කළ (අඟල් 1 – 3 අතර) රැෂිග් වලයයන් හෝ හැඩගැන්වු ලෝහ තහඩු විය හැකිය. ඇසුරුම් ද්රව්යයේ පෘෂ්ටය ද්රව මගින් තෙත් වන අතර මෙම තෙත් වු පෘෂ්ටය මතින් වාෂ්ප ගමන් කරයි. එහිදි ස්කන්ධ හුවමාරුව සිදුවේ. සාමාන්යයෙන් භාවිත වන එක් එක් මට්ටමක් මගින් එකිනෙකට වෙනස් ද්රව - වාෂ්ප සමතුලිතතා ලක්ෂ්යයක් දෙනු ලබන බහුමට්ටම් ආසවන කුළුණු මෙන් නොව අසුරන ලද කුළුණක් තුල ද්රව - වාෂ්ප සමතුලිතතා වක්රය සංතතික වේ. නමුත් අසුරන ලද කුළුණු ආදර්ශනයේදී සෛද්ධාන්තික මට්ටම් කිහිපයක් ගණනය කිරීම සාමාන්ය ආකාරයේ මට්ටම් සහිත කුළුණකට සාපේක්ෂව ඒවායේ විභාජක කාර්යක්ෂමතාවය දැක්වීම සඳහා වැදගත් වේ. විවිධාකාරයෙන් හැඩ ගන්වන ලද ඇසුරුම් ද්රව්ය වල ක්ෂේත්ර ඵලයන් එකිනෙකට වෙනස් වන අතර ඇසුරුම් ද්රව්යයන් අතර පවතින අවකාශද විශාලත්වයෙන් එකිනෙකට වෙනස් වේ. මෙම ගුණාංග යුගලම ඇසුරුම් ද්රව්යවල කාර්යක්ෂමතාව සඳහා බලපායි.
විශේෂ ආකාරයකට ඇසුරුම් නොකළ හෝ හැඩ ගැන්වු ඇසුරුම් භාවිතා වන ආසවන කුළුණක ක්රියාකාරිත්වය සඳහා ඇසුරුම් හැඩය සහ ක්ෂේත්ර ඵලය හැරුනු විට ඇසුරුම් ස්ථරයට ඇතුල් වන ද්රව සහ වාෂ්ප ව්යාප්තිය බලපායි. දෙන ලද විභාජනයක් සිදු කිරීම සඳහා අවශ්ය වන සෛද්ධාන්තික මට්ටම් සංඛ්යාව නිෂ්චිත වාෂ්ප ද්රව අනුපාතයක් ඇසුරින් ගණනය කෙරේ. ඇසුරුම් ස්ථරයට ඇතුල් වන විට ද්රව සහ වාෂ්ප කුළුනු පෘෂ්ටය හරහා ඒකාකාරව ව්යාප්ත වී නොමැති විට ඇසුරුම් ස්ථරය තුළ ද්රව වාෂ්ප අනුපාතය නිරවද්ය නොවන අතර ඉලක්ක ගත විභාජනය සිදුනොවේ. ඇසුරුම් ද්රව්ය නිසි පරිදි ක්රියා නොකරන බව මෙවිට හැඟී යනු ඇත. සෛද්ධාන්තික මට්ටමකට තුල්ය උස අදහස් කරන අගයට වඩා ඉහළ අගයක් ගනු ඇත. මෙහිදි ගැටළුව වන්නේ ඇසුරුම් ද්රව්ය නොව එම ස්ථරයට ඇතුල් වන තරලයන් විසිරි ඇති ආකාරයයි. බහුල වශයෙන් වැරදි ලෙස ව්යාප්ත වන්නේ වාෂ්පය නොව ද්රවයයි. සැපයුම සහ ප්රතිවාහය ඇසුරුම් ස්ථරයට ඇතුල් කිරීමට භාවිතා වන ද්රව ව්යාප්තක නිර්මාණය කර ඇති ආකාරයෙන් ඇසුරුම් උපරිම කාර්යක්ෂමතාවයෙන් ක්රියාකිරීම සඳහා අතිශය වැදගත් වේ. ඇසුරුම් ස්ථරයකට ඇතුල් වන ද්රවය ඒකාකාරව විසිරවීම සඳහා ද්රව ව්යාප්තකයකට ඇති හැකියාව ගණනය කිරීමේ ක්රම යොමුවෙහි සඳහන් වෙයි. මෙම මාතෘකාව සම්බන්ධයෙන් විශාල වැඩ කොටසක් Fractionatrion Research, Inc. (FRI) මගින් සිදු කර ඇත.